【题目】合成氨工业涉及固体燃料的气化,需要研究CO2与CO之间的转化。为了弄清其规律,让一定量的CO2与足量碳在体积可变的密闭容器中反应C(s)+CO2(g)2CO(g) ΔH,测得压强、温度对CO、CO2的平衡组成的影响如图所示:
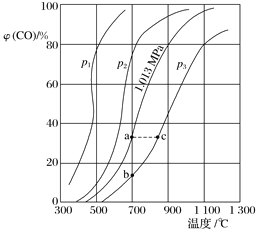
(1)p1、p2、p3的大小关系是_______,欲提高C与CO2反应中CO2的平衡转化率,应采取的措施为___________________。图中a、b、c三点对应的平衡常数(用Ka、Kb和Kc表示)大小关系是____________________;
(2)900 ℃、1.013 MPa时,1 mol CO2与足量碳反应达平衡后容器的体积为V,CO2的转化率为__________,该反应的平衡常数K=________________。
(3)将(2)中平衡体系温度降至640 ℃,压强降至0.101 3 MPa,重新达到平衡后CO2的体积分数为50%。条件改变时,正反应和逆反应速率如何变化?_________________,二者之间有何关系?__________________。
(4)CO2催化加氢也可转化为CO,但同时会合成二甲醚,其过程中主要发生下列反应:
反应Ⅰ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=41.2 kJ·mol-1
反应Ⅱ:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ΔH=-122.5 kJ·mol-1
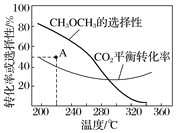
在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图
其中:CH3OCH3的选择性=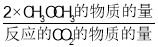 ×100%
×100%
①温度高于300 ℃,CO2平衡转化率随温度升高而上升的原因是___________;
②220 ℃时,在催化剂作用下CO2与H2反应一段时间后,测得CH3OCH3的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高CH3OCH3选择性的措施有________________。
(5)水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用*标注。
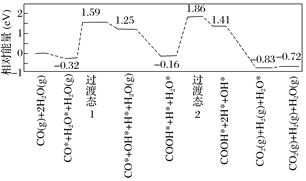
可知水煤气变换的ΔH_______0(填“大于”、“等于”或“小于”)。该历程中最大能垒(活化能)E正=_______eV,写出该步骤的化学方程式____________________。
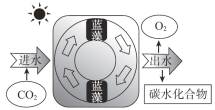
![]() 碳水化合物+ O ,该系统利用了蓝藻的光合作用,故A正确;
碳水化合物+ O ,该系统利用了蓝藻的光合作用,故A正确;![]() 碳水化合物+ O ,反应消耗水,理论上系统出水量小于进水量,故B正确;
碳水化合物+ O ,反应消耗水,理论上系统出水量小于进水量,故B正确;
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案