题目内容
【题目】下列说法正确的是
①符合通式CnH2n+2 的烃一定都是烷烃,分子中均只含单键
②苯能使溴水褪色,说明苯环结构中含有碳碳双键
③乙酸与油酸一定不是同系物
④乙烯能使溴水和酸性KMnO4 溶液褪色,且反应类型相同
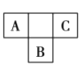
⑤![]() 与
与![]() 是同分异构体
是同分异构体
⑥相同质量的烃完全燃烧,耗氧量最大的是 CH4
⑦戊二酸的分子式是C5H8O4,符合此分子式的二元酸有 3 种
A.①③⑦B.①③⑥C.②⑥⑦D.④⑤⑦
【答案】B
【解析】
①CnH2n+2为烷烃的通式,分子中只含单键,故①正确;
②苯能使溴水褪色,发生了萃取,属于物理变化;苯与溴水不反应,苯能使溴水褪色,不说明苯环结构中含有碳碳双键,故②错误;
③油酸含有碳碳双键,而乙酸不含,所以二者一定不是同系物,故③正确;
④乙烯使溴水褪色是因为发生加成反应,使酸性高锰酸钾褪色是因为被氧化,反应类型不同,故④错误;
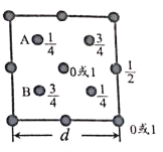
⑤因为甲烷是正四面体结构,所以其二氯代物只有一种,即![]() 与
与![]() 是同种物质,故⑤错误;
是同种物质,故⑤错误;
⑥相同质量的烃完全燃烧,含氢量越大,耗氧量越大,烃中甲烷中含氢量最大,则甲烷耗氧量最大,故⑥正确;
⑦戊二酸可以看作2个-COOH取代丙烷中的2个H原子,取代同一碳原子上的2个H原子有2种结构,取代不同C原子上H原子有2种结构,符合此分子式的戊二酸有4种,故⑦错误;
综上所述正确的有①③⑥,故答案为B。

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目