题目内容
有等体积、等pH的Ba(OH)2、NaOH和NH3·H2O三种碱溶液,滴加等物质的量浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是( )
| A.V3>V2>V1 | B.V1=V2=V3 |
| C.V3>V2=V1 | D.V1=V2>V3 |
C
解析试题分析:等体积、等pH的Ba(OH)2、NaOH和NH3·H2O三种碱溶液,溶液中的OH?浓度相同,因为Ba(OH)2、NaOH为强碱,NH3?H2O为弱碱,则NH3?H2O 浓度远远大于Ba(OH)2和NaOH,所以用去酸的体积为:V3>V2=V1,故C项正确。
考点:本题考查

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
将下列溶液分别蒸干并灼烧,能得到溶质的是
| A.FeCl3 | B.AlCl3 | C.Na2CO3 | D.NaHCO3 |
对于常温下PH为2的盐酸,叙述正确的是
| A.c(H+) = c(Cl—) + c(OH—) |
| B.由H2O电离出的c(H+) =" 1.0" ×10—12 mol·L—1 |
| C.与等体积PH=12的氨水混合后所得溶液显酸性 |
| D.与等体积0.01 mol·L—1乙酸钠溶液混合后所得溶液中:c(Cl—) = c(CH3COO—) |
AgCl(s)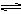 Ag+(aq) + Cl-(aq),平衡时,Ksp =C(Ag+ )·C(Cl-) ,过量氯化银分别投入①100 mL水 ②24 mL 0.1 mol·L-1NaCl ③10 mL 0.1 mol·L-1MgCl2 ④30 mL 0.1 mol·L-1AgNO3溶液中,溶液中C(Ag+)由大到小顺序为
Ag+(aq) + Cl-(aq),平衡时,Ksp =C(Ag+ )·C(Cl-) ,过量氯化银分别投入①100 mL水 ②24 mL 0.1 mol·L-1NaCl ③10 mL 0.1 mol·L-1MgCl2 ④30 mL 0.1 mol·L-1AgNO3溶液中,溶液中C(Ag+)由大到小顺序为
| A.③①②④ | B.④①②③ | C.①②③④ | D.④③②① |
根据下列实验内容得出的结论正确的是
| | 实验操作 | 解释或结论 |
| A |  沉淀中滴入浓KCI溶液有白色沉淀出现 沉淀中滴入浓KCI溶液有白色沉淀出现 |  比 比 更难溶 更难溶 |
| B | 某物质的水溶液能使红色石蕊试纸变蓝 | 该物质一定是氨气 |
| C | 滴加氯水和 振荡,静置,下层溶液为紫色 振荡,静置,下层溶液为紫色 | 原溶液中有 |
| D | 用洁净的铂丝蘸取溶液进行焰色反应,火焰呈黄色 | 含有Na单质 |
H2S水溶液中存在电离平衡H2S H++HS– 和HS–
H++HS– 和HS– H++S2–。下列说法正确的是
H++S2–。下列说法正确的是
| A.加水,平衡向右移动,溶液中氢离子浓度增大 |
| B.通入过量SO2气体,平衡向左移动,溶液pH值增大 |
| C.滴加新制氯水,平衡向左移动,溶液pH值减小 |
| D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小 |
室温下,下列溶液等体积混和,所得溶液pH的一定大于7的是( )
| A.0.1mol.l-1盐酸溶液和0.1mol.l-1氢氧化钠溶液 |
| B.0.1mol.l-1盐酸溶液和0.1mol.l-1氢氧化钡溶液 |
| C.pH =4醋酸溶液和pH =10氢氧化钠溶液 |
| D.pH =4盐酸溶液和pH =10氢氧化钡溶液 |
相同物质的量浓度的NaCN 和NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN 和HClO说法正确的是
| A.酸根离子浓度:c(CNˉ)<c(ClOˉ) |
| B.电离程度:HCN>HClO |
| C.pH:HClO>HCN |
| D.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
室温时,0.1mo1/L某一元酸HA在水中有1%发生电离,下列叙述不正确的是
A.该溶液的pH= 3 3 | |
B.由HA电离出的c(H+)约为水电离出的c(H+)的108倍 | C.Na2A溶液显碱性 |
D.升高温度,溶液的pH增大 |