题目内容
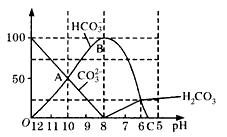
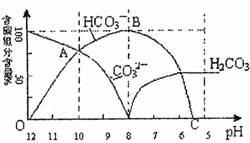
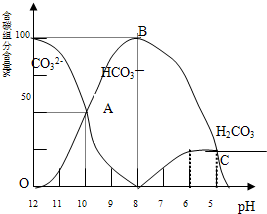 常温下在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示:回答下列问题:
常温下在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示:回答下列问题:(1)20mL 0.1mol/LNa2CO3溶液呈碱性的原因是(用离子方程式表示)
(2)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO32-离子不超过其总量的10%.请你设计简单实验证明该同学的观点是否正确
(3)若向20mL 0.1mol/LNa2CO3溶液中加入BaCl2粉末3.328×10-7g时开始产生沉淀X,则Ksp(X)=
(4)请写出OAB段的离子方程式
分析:(1)碳酸钠是强碱弱酸盐,碳酸根离子水解而使其溶液呈碱性;任何电解质溶液中都存在电荷守恒;
(2)用pH试纸或pH计测定常温下0.1mol/L碳酸钠溶液的pH来确定;
(3)根据KSP(BaCO3)=c(Ba2+)×c(CO32-)计算;
(4)OAB段碳酸氢根离子浓度增大,碳酸根离子浓度减小,说明碳酸根离子和氢离子反应生成碳酸氢根离子;当溶液中H2CO3达到饱和后,开始放出CO2气体.
(2)用pH试纸或pH计测定常温下0.1mol/L碳酸钠溶液的pH来确定;
(3)根据KSP(BaCO3)=c(Ba2+)×c(CO32-)计算;
(4)OAB段碳酸氢根离子浓度增大,碳酸根离子浓度减小,说明碳酸根离子和氢离子反应生成碳酸氢根离子;当溶液中H2CO3达到饱和后,开始放出CO2气体.
解答:解:(1)碳酸钠是强碱弱酸盐,碳酸根离子水解而使其溶液呈碱性,水解方程式为:CO32-+H2O?HCO3-+OH-;任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)=2c (CO32-)+c(HCO3-)+c (OH-),
故答案为:CO32-+H2O?HCO3-+OH-;c(Na+)+c(H+)=2c (CO32-)+c(HCO3-)+c (OH-);
(2)用pH试纸或pH计测定常温下0.1mol/L碳酸钠溶液的pH来确定,若pH<12,则该同学的观点正确;若pH>12,则该同学的观点不正确,
故答案为:用pH试纸(或pH计)测常温下0.1mol?L-1 Na2CO3溶液的pH,若pH<12,则该同学的观点正确,若pH>12,则该同学的观点不正确;
(3)该溶液中钡离子浓度=
=8.0×10-8 mol/L,K=0.1×8.0×10-8=8.0×10-9,故答案为:8.0×10-9;
(4)Na2CO3溶液中加入少量盐酸生成HCO3-,反应的离子方程式为CO32-+H+=HCO3-,当溶液中H2CO3达到饱和后,开始放出CO2气体,由图象可以看出,当pH=6时,H2CO3达到饱和,开始放出CO2气体,故答案为:CO32-+H+=HCO3-;6.
故答案为:CO32-+H2O?HCO3-+OH-;c(Na+)+c(H+)=2c (CO32-)+c(HCO3-)+c (OH-);
(2)用pH试纸或pH计测定常温下0.1mol/L碳酸钠溶液的pH来确定,若pH<12,则该同学的观点正确;若pH>12,则该同学的观点不正确,
故答案为:用pH试纸(或pH计)测常温下0.1mol?L-1 Na2CO3溶液的pH,若pH<12,则该同学的观点正确,若pH>12,则该同学的观点不正确;
(3)该溶液中钡离子浓度=
| ||
| 0.02L |
(4)Na2CO3溶液中加入少量盐酸生成HCO3-,反应的离子方程式为CO32-+H+=HCO3-,当溶液中H2CO3达到饱和后,开始放出CO2气体,由图象可以看出,当pH=6时,H2CO3达到饱和,开始放出CO2气体,故答案为:CO32-+H+=HCO3-;6.
点评:本题考查溶液离子浓度大小比较以及难溶电解质的溶解平衡及沉淀转化等问题,题目难度中等,注意分析图象曲线变化趋势,把握物质的性质.

练习册系列答案
相关题目
在常温下向20mL 0.1 mol·L-1 某酸(用HAc表示)溶液中逐滴加入0.1 mol·L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化)。请根据表中数据和滴定曲线回答以下问题:
|
V(NaOH)mL |
0.00 |
10.00 |
18.00 |
19.80 |
19.98 |
20.00 |
20.02 |
20.20 |
22.00 |
40.00 |
|
pH |
3.0 |
4.7 |
5.7 |
6.7 |
7.7 |
8.7 |
9.7 |
10.7 |
11.7 |
12.5 |
(1)实验中的指示剂最好使用___________________________;
(2)当V (NaOH)=20.00mL时,请写出溶液中主要存在的两种平衡状态的表示式_______________、________________;溶液中离子浓度由大到小的顺序是___________________;
(3)a、b、c、d四点对应溶液中水的电离程度由大到小的顺序是_________________。
(4)该温度下,滴定曲线上c点时HAc的电离平衡常数Ka=_______(用含V的代数简式表示)。