题目内容
【题目】现有 A、B、C、D、E、F、G、H 八种元素,均为前四周期元素,它们的原子序数依次增大。 请根据下列相关信息,回答有关问题。
A 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素
B 元素是形成化合物种类最多的元素
C 元素基态原子的核外 p 电子数比 s 电子数少 1
D 元素基态原子的核外 p 轨道中有两个未成对电子
E 元素的气态基态原子的第一至第四电离能分别是 I1=738 kJ/mol,I2=1451 kJ/mol,I3=7733 kJ/mol,I4=10540 kJ/mol
F 元素的主族序数与周期数的差为 4
G 元素是前四周期中电负性最小的元素
H 元素位于元素周期表中的第八纵行
(1)C2A4 的电子式为__________ (A、C 为字母代号,请将字母代号用元素符号表示,下同)。
(2)B 元素的原子核外共有__________种不同运动状态的电子。
(3)某同学推断 E 元素基态原子的核外电子排布图为 ![]() 。该同学所画的电子排布图违背了_________,该元素原子的 I3 远远大于 I2,其原因是____________________。
。该同学所画的电子排布图违背了_________,该元素原子的 I3 远远大于 I2,其原因是____________________。
(4)D、E、F 三种元素的简单离子半径由大到小的顺序是__________ (用离子符号表示)。
(5)用惰性电极电解 EF2 的水溶液的离子方程式为__________。
(6)H 位于元素周期表中__________区(按电子排布分区),其基态原子的价电子排布式为_________,实验室用一种黄色溶液检验 H2+时产生蓝色沉淀,该反应的离子方程式为____________________。
【答案】![]() 6 泡利原理 Mg原子失去2个电子后形成稳定结构,此时再失去1个电子很困难 Cl>O2>Mg2+ Mg2++2Cl+2H2O
6 泡利原理 Mg原子失去2个电子后形成稳定结构,此时再失去1个电子很困难 Cl>O2>Mg2+ Mg2++2Cl+2H2O![]() Mg(OH)2↓+Cl2↑+H2↑ d 3d64s2 3Fe2++2[Fe(CN)6]3=Fe3[Fe(CN)6]2↓
Mg(OH)2↓+Cl2↑+H2↑ d 3d64s2 3Fe2++2[Fe(CN)6]3=Fe3[Fe(CN)6]2↓
【解析】
现有A、B、C、D、E、F、G、H八种元素,均为前四周期元素,它们的原子序数依次增大。A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素,则A为H元素;B元素是形成化合物种类最多的元素,则B为C元素;C元素原子的核外p电子数比s电子数少1,则C为N元素;D元素基态原子的核外p轨道中有两个未成对电子,其电子排布为1s22s22p4,则D为O元素;G元素是前四周期中电负性最小的元素,则G为K元素;E原子的第一到第四电离能分别是:I1=738kJ/mol、I2=1451kJ/mol、I3=7733kJ/mol、I4=10540kJ/mol,说明E最外层有2个电子,其原子序数小于K,则E为Mg元素;F元素的主族序数与周期数的差为4,其原子序数大于Mg,则F位于第三周期,最外层含有7个电子,为Cl元素;H元素位于元素周期表中的第八列,为前四周期元素,且原子序数大于K,则H为Fe元素,据此解答。
(1)C2A4为N2H4,N2H4为共价化合物,其电子式为![]() ;
;
(2)B为C元素,核外电子总数=原子序数=6,每个电子的运动状态都不同,则C原子有6种不同的运动状态;
(3)![]() 中3s能级的2个电子自旋方向相同,违背了泡利原理;由于Mg原子失去2个电子后形成稳定结构,此时再失去1个电子很困难,则Mg元素的原子I3远远大于I2;
中3s能级的2个电子自旋方向相同,违背了泡利原理;由于Mg原子失去2个电子后形成稳定结构,此时再失去1个电子很困难,则Mg元素的原子I3远远大于I2;
(4)电子层越多离子半径越大,电子层相同时,核电荷数越大离子半径越小,则离子半径大小为:Cl>O2>Mg2+;
(5)用惰性电极电解MgCl2的水溶液,阳极氯离子放电,阴极水电离的氢离子放电,该反应的离子方程式为:Mg2++2Cl+2H2O![]() Mg(OH)2↓+Cl2↑+H2↑;
Mg(OH)2↓+Cl2↑+H2↑;
(6)H为Fe元素,位于元素周期表中的d区,Fe元素的原子序数为26,其基态原子的价电子排布式为3d64s2;实验室用一种黄色溶液检验Fe2+时产生蓝色沉淀,该反应的离子方程式为:3Fe2++2[Fe(CN)6]3=Fe3[Fe(CN)6]2↓。

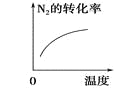
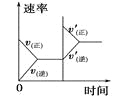
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g) △H<0,下列研究目的和示意图相符的是( )
2NH3(g) △H<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响 (p2>p1) | 温度对反应的影响 | 平衡体系中增加N2的浓度对反应的影响 | 催化剂对反应的影响 |
示意图 |
|
|
|
|
A.AB.BC.CD.D