题目内容
Ⅰ:某些化学反应可表示为:A+B→C+D+H2O,请回答下列问题:
(1)若A、C、D均是铁的化合物,B是稀硫酸,则A与B反应的化学方程式为
(2)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,该反应离子方程式为 。
(3)若A为淡黄色固体,C为无色的气体,则该反应的离子方程式为 。
Ⅱ:某些化学反应可表示为:A+NaOH+H2O→C+D。请回答下列问题:
(1)若A为金属单质,C为非金属单质,写出符合要求的离子方程式_____________________
(2)若A为非金属单质,C为非金属单质,写出符合要求的化学反应方程式
(其它合理也可)
Ⅰ(1)Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
(2)Cl2+2OH-=Cl-+ClO-+H2O
(3)2Na2O2+4H+=O2↑+4Na+ +2H2O
Ⅱ(1)2Al+2OH-+2H2O= 2AlO2-+3H2↑
(2)Si+2NaOH+H2O= Na2SiO3+2H2↑
解析试题分析:Ⅰ(1)分析反应特点,结合A、C、D均是铁的化合物,可知A是Fe3O4,则A与B反应的化学方程式为: Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
(2)A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,猜想A是氯气,与碱液的反应,离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O
(3)A为淡黄色固体,则A为过氧化钠,产物有三种,可考虑为过氧化钠与酸的反应,离子方程式为:2Na2O2+4H+=O2↑+4Na+ +2H2O
Ⅱ根据反应特点,与氢氧化钠溶液反应的单质中有铝、硅,
(1)A为铝,离子方程式为2Al+2OH-+2H2O= 2AlO2-+3H2↑;
(2)A为硅,化学方程式为Si+2NaOH+H2O= Na2SiO3+2H2↑
考点:考查对化学方程式的特点的分析能力、对某些特殊物质的化学性质的熟悉度

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案下列实验操作及现象能够达到对应实验目的的是
| 选项 | 实验操作及现象 | 实验目的 |
| A | 将SO2通入品红溶液中,品红溶液褪色;加热褪色后的品红溶液,溶液恢复红色 | 验证亚硫酸的不稳定性 |
| B | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有少量气泡产生 | 证明常温下 Ksp(BaCO3)>Ksp(BaSO4) |
| C | 常温下,测定物质的量浓度相同的盐酸和醋酸溶液的pH:盐酸pH小于醋酸pH | 证明相同条件下,在水溶液中HCl电离程度大于CH3COOH |
| D | 将浓硫酸与碳混合加热,直接将生成的气体通入足量的石灰水,石灰水变浑浊 | 检验气体产物中CO2的存在 |
稀土元素是周期表中Ⅲ B族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合价为+3。其中钇(Y)元素是激光和超导的重要材料。
我国蕴藏着丰富的钇矿石( Y2 FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下: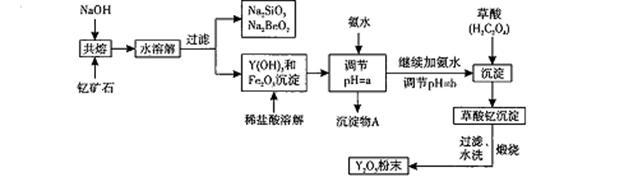
已知:
I.有关金属离子形成氢氧化物沉淀时的pH如下表:
| | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
Ⅱ.在周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)钇矿石(Y2 FeBe2Si2O10)的组成用氧化物的形式可表示为 。
(2)欲从Na2 SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀。则
①最好选用盐酸、 (填字母代号)两种试剂,再通过必要的实验操作方可实现。
a.NaOH溶液 b.氨水 c.CO2气 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式: :必要的实验操作应是 。
(3)为使Fe3+沉淀完全,须用氨水调节pH =a,则a应控制在 的范围内;继续加氨
水调节pH =b发生反应的离子方程式为 ,溶液中Fe3+完全沉淀的判定标准是 。
(4)写出草酸钇[Y2(C2O4)3.Nh2O]煅烧的化学方程式 。
工业上利用软锰矿(主要成分为MnO2,同时含少量铁、铝等的化合物)制备硫酸锰的常见流程如下: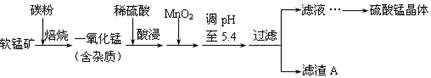
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 |
(1)一氧化锰用硫酸酸浸时发生的主要反应的离子方程式为____________________。酸浸后加入MnO2将溶液中的Fe2+氧化成Fe3+,其目的是___________。
(2)滤渣A的成分除MnO2外,还有_______________。
(3)MnO2是制造碱性锌锰电池的基本原料,放电时负极的电极反应式为________。工业上以石墨为电极电解酸化的MnSO4溶液生产MnO2,阳极的电极反应式为_________,当阴极产生4.48L(标况)气体时,MnO2的理论产量为______g。
(4)锰的三种难溶化合物的溶度积:Ksp(MnCO3)=1.8×10-11,Ksp[Mn(OH)2]=1.9×10-13,Ksp(MnS)=2.0×10-13,则上述三种难溶物的饱和溶液中,Mn2+浓度由大到小的顺序是_______>_______>_______(填写化学式)。
同一主族的两种元素的原子序数之差不可能的是
| A.16 | B.26 | C.36 | D.46 |
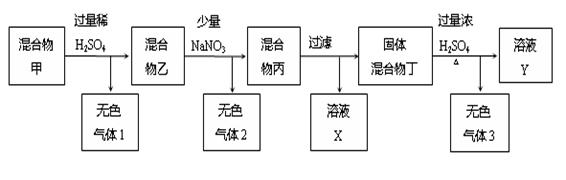
 、X中的一种。
、X中的一种。 C.CH3COO D.SiO
C.CH3COO D.SiO