题目内容
【题目】如图所示曲线a和b是盐酸与氢氧化钠溶液相互滴定的滴定曲线,下列叙述正确的是( )

A.P点时恰好完全反应,溶液呈中性
B.盐酸的物质的量浓度为1 mol·L-1
C.酚酞不能用作本实验的指示剂
D.曲线a是盐酸滴定氢氧化钠溶液的滴定曲线
【答案】A
【解析】
据图知,未加溶液时,a曲线的pH=1,说明该实验是将NaOH滴定稀盐酸,b曲线的pH=13,该实验是将稀盐酸滴定NaOH;
A.P点时二者恰好完全中和,盐酸是一元强酸,氢氧化钠是一元强碱,当二者恰好中和时,二者反应生成氯化钠,则溶液呈中性,故A正确;
B.根据图象知,当盐酸中未滴加氢氧化钠溶液时,溶液的pH=1,则c(HCl)=c(H+)=10-1 mol/L=0.1mol/L,故B错误;
C.甲基橙的变色范围是3.1-4.4,酚酞的变色范围是8-10,且变色现象较明显,所以该中和滴定可以用酚酞或甲基橙作指示剂,故C错误;
D.根据图象知,当a曲线发生中和反应时,溶液的pH=1,说明原溶液是盐酸,所以a曲线是氢氧化钠滴定盐酸的实验,故D错误;
故答案为A。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】现使用酸碱中和滴定法测定市售白醋的总酸量g/100ml![]() 。
。
(1)量取10.00ml食用白醋,在烧杯中用水稀释后转移到100mL容量瓶中定容,摇匀即得待测白醋溶液。
(2)用___(填仪器名称)取待测白醋溶液20.00ml于锥形瓶中,向其中滴加2滴酚酞。
(3)读取盛装0.1000mol/LNaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为___mL。滴定终点的现象:___,停止滴定,记录NaOH溶液的终读数,计算实验所用NaOH溶液总体积记录于下表,重复滴定4次。
![]()
(4)实验记录数据(ml)
滴定次数 | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH) | 15.95 | 15.00 | 15.05 | 14.95 |
(5)数据处理与讨论:
A.甲同学在处理数据时计算得:平均消耗的NaOH溶液的体积__ml,按正确数据处理,可得市售白醋总酸量![]() __g/100ml。
__g/100ml。
B.在本实验的滴定过程中,下列操作对实验结果的影响是(填写“偏大”、“偏小”或“无影响”)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗___;
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失___;
c.锥形瓶中加入待测白醋溶液后,再加少量水___。
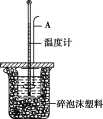
【题目】测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示。
(1)理论上强酸强碱的稀溶液反应生成1 mol水时放出57.3 kJ的热量,写出表示稀硫酸和氢氧化钠稀溶液反应的中和热的热化学方程式: ____________________。
(2)仪器A的名称是 _____________;在实验过程中,如果不把温度计上的酸用水冲洗干净就直接测量NaOH溶液的温度,则测得的ΔH_____________ (填“偏大”“偏小”或“无影响”)。
(3)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白: ___________
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3中和后生成溶液的比热容c=4.18 J/(g·℃)则中和热ΔH= _____________(取小数点后一位)
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是_____________ (填序号)。
a.实验装置保温隔热效果差
b.用量筒量取NaOH溶液的体积时仰视读数
c.分多次把NaO溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度