题目内容
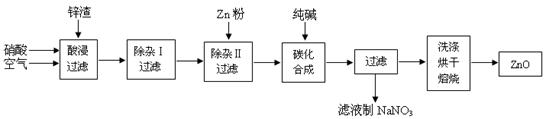
氧化锌粉末广泛应用于橡胶、涂料、陶瓷、化工、医药、玻璃等行业,为综合应用资源,常从冶炼锌、锌制品加工企业回收的锌渣(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质)来制取氧化锌,流程如图:
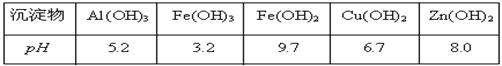
有关氢氧化物沉淀完全的pH见下表:
(1)在酸浸过程中,常将锌渣碎成粉末并通入空气,同时保持酸过量,理由是 。
(2)上述工艺多处涉及“过滤”,实验室中过滤需要使用的玻璃仪器有烧杯、 。
(3)①在“除杂Ⅰ”中,常用酸性KMnO4溶液,其目的是 ,KMnO4是该反应的 (氧化剂、还原剂)。将溶液的pH调至4,目的是 。
②在“除杂II”中,加入锌粉的目的是 。
(4)在“碳化合成”中,产物中有碱式碳酸锌[Zn2(OH)2CO3]和CO2等,请写出该反应的化学方程式 。
(5)本工艺中,过滤分离次数较多,其明显的缺陷是 。

有关氢氧化物沉淀完全的pH见下表:

(1)在酸浸过程中,常将锌渣碎成粉末并通入空气,同时保持酸过量,理由是 。
(2)上述工艺多处涉及“过滤”,实验室中过滤需要使用的玻璃仪器有烧杯、 。
(3)①在“除杂Ⅰ”中,常用酸性KMnO4溶液,其目的是 ,KMnO4是该反应的 (氧化剂、还原剂)。将溶液的pH调至4,目的是 。
②在“除杂II”中,加入锌粉的目的是 。
(4)在“碳化合成”中,产物中有碱式碳酸锌[Zn2(OH)2CO3]和CO2等,请写出该反应的化学方程式 。
(5)本工艺中,过滤分离次数较多,其明显的缺陷是 。
(1)增大反应面积,加快反应速率(2分);保证锌渣充分反应。(1分)
(2)玻璃棒、漏斗 (2分,漏写一个得1分)
(3)①将Fe2+转化成为Fe3+(2分),氧化剂(1分) 使Fe3+ 完全转化为Fe(OH)3沉淀(2分)
②除去溶液中的Cu2+(或调节溶液的pH值)(2分)
(4)2Na2CO3+2Zn(NO3)2+H2O=4NaNO3+Zn2(OH)2CO3+CO2↑(2分,未配平扣1分)
(5)过滤次数较多,锌元素损失较多(2分)
(2)玻璃棒、漏斗 (2分,漏写一个得1分)
(3)①将Fe2+转化成为Fe3+(2分),氧化剂(1分) 使Fe3+ 完全转化为Fe(OH)3沉淀(2分)
②除去溶液中的Cu2+(或调节溶液的pH值)(2分)
(4)2Na2CO3+2Zn(NO3)2+H2O=4NaNO3+Zn2(OH)2CO3+CO2↑(2分,未配平扣1分)
(5)过滤次数较多,锌元素损失较多(2分)
试题分析:(1)酸浸采取的措施与加快反应速率、提高浸出率或原料的利用率;
(2)过滤需要漏斗、玻璃棒、烧杯等玻璃仪器;
(3)酸性高锰酸钾溶液具有强氧化性,将Fe2+转化成为Fe3+,调节pH使Fe3+ 完全转化为Fe(OH)3沉淀;锌比铜活泼,可以除去溶液中的Cu2+(或调节溶液的pH值);
(4)由原子守恒可知,2Na2CO3+2Zn(NO3)2+H2O=4NaNO3+Zn2(OH)2CO3+CO2↑;
(5)过滤次数较多,锌元素损失较多,降低产率。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目