题目内容
为了在实验室模拟用二氧化氮溶于水生成硝酸,现进行如下实验:
实验一:制备并收集一试管二氧化氮
(1)实验室常用浓硝酸与铜反应制备二氧化氮,化学方程式是________
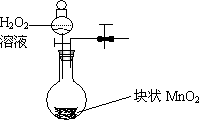
(2)可用下图装置制备并收集一试管二氧化氮,
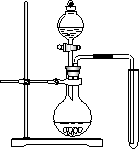
①在加入药品前,必须进行的操作是________.
②该装置的缺点是(只填一个缺点既可)________.
实验二:尽可能多地使试管中的二氧化氮被水吸收
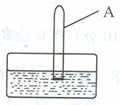
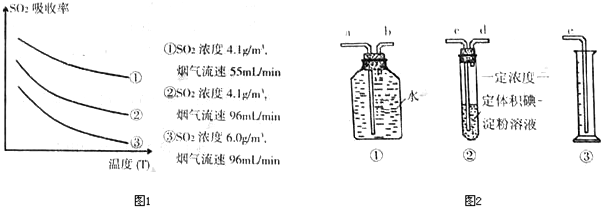
(3)将装有二氧化氮的试管A倒插入水中(图Ⅱ),并轻轻晃
动试管,观察到的现象是:________.
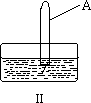
(4)从下图中挑选所需的仪器,完成制取O2,并将O2通入到上述实验后的试管A中.
①画出制取O2装置简图(添加必要的塞子、玻璃导管、胶皮管.固定装置不用画),并标明所用试剂.
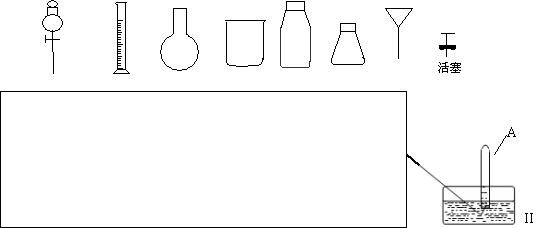
②某同学在试管A内通入O2的过程中没有观察到液面上升,而是试管内充满了无色气体,可能原因是________.
答案:
解析:
解析:
(1)Cu+4HNO3(浓)![]() Cu(NO3)2+2NO2↑+2H2O(2分);
Cu(NO3)2+2NO2↑+2H2O(2分);
(2)①检查装置的气密性(1分)
②没有尾气处理装置,过量的NO2逸出后将导致空气污染.(2分)
(或:不能随时控制反应的开始和停止,浪费药品,且过量的NO2逸出后将导致空气污染)
(3)试管内液面上升到约为试管体积的2/3,气体由棕红色变为无色.(2分)
3NO2+H2O![]() 2HNO3+NO(2分)
2HNO3+NO(2分)
(4)①

(4分)[4分,其中药品选择合理1分,仪器绘制正确1分,仪器连接正确2分(胶塞、活塞各1分)]
②O2通入的速度过快,导致试管内迅速充满了O2.(2分)

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
(6分)通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能. 已知部分化学键的键能如下:
| 化学键 | N—H | N—N | O==O | N≡N | O—H |
| 键能(kJ/mol) | 386 | 167 | 498 | 946 | 460 |
(2)为了提高肼(N2H4)燃烧过程中释放的能量,常用二氧化氮作氧化剂代替氧气,这两者反应生成氮气和水蒸气.且:
①N2(g)+2O2(g)===2NO2(g) ΔH1=+67.7 kJ/mol
②N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH2=-534 kJ/mol
试写出肼和NO2完全反应的热化学方程式:____________________________________
(3)随着中国空间技术的发展,中俄于2009年携手探火星工程,寻找更高效的火箭推进剂也被提到了议事日程.在实验室我国科研人员应用电子计算机模拟出具有高能量的物质N60,它的结构与C60十分相似.已知N60分子中每个N原子均以氮氮键结合三个氮原子,且N60分子结构中每个氮原子均形成8个电子的稳定结构.试推测1个N60的结构含有________个N—N键.
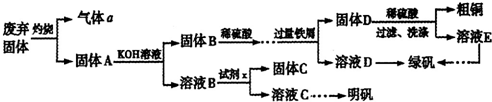
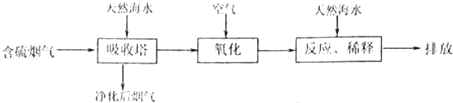
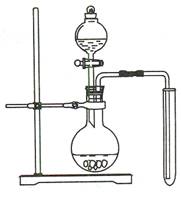 实验I:制备并收集一试管二氧化氮
实验I:制备并收集一试管二氧化氮