题目内容
(2013?淄博二模)实验室模拟用工业废弃固体(含有Cu2S、Al2O3、Fe2O3、SiO2等)制取粗铜、绿矾(FeSO4?7H2O)和明矾[Kal(SO4)2?12H2O]的操作流程如下:
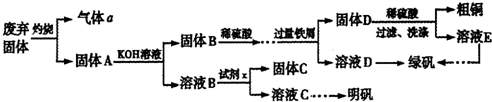
(1)试剂x是
(2)配平下列方程式:
(3)为了分析产品(绿矾)中铁元素的含量,某同学称取20.0g样品配成100mL溶液,移取25.00mL用1.000×10-1mol?L-1KMnO4标准溶液进行滴定(MnO4-被还原为Mn2+).
请回答下列问题:
①滴定时,KmnO4标准溶液应盛放在
②若达到滴定终点消耗KmnO4标准溶液体积为25.00mL,则该产品中铁元素的质量分数为

(1)试剂x是
H2SO4(或KHSO4)
H2SO4(或KHSO4)
(写化学式).(2)配平下列方程式:
2
2
MnO4-+5
5
SO2+2
2
H2O=Mn2+5
5
SO42-4
4
H+(3)为了分析产品(绿矾)中铁元素的含量,某同学称取20.0g样品配成100mL溶液,移取25.00mL用1.000×10-1mol?L-1KMnO4标准溶液进行滴定(MnO4-被还原为Mn2+).
请回答下列问题:
①滴定时,KmnO4标准溶液应盛放在
酸式滴定管
酸式滴定管
(填仪器名称)中.②若达到滴定终点消耗KmnO4标准溶液体积为25.00mL,则该产品中铁元素的质量分数为
14%
14%
.分析:(1)根据产物与反应物的特点进行分析;
(2)根据化合价升降法即可配平化学方程式;
(3)氧化还原反应的计算原则是电子得失总数相等,得出KMnO4与Fe2+的对应关系,由KMnO4求出Fe2+的量,因为样品配成了100mL溶液,滴定时取用了25.00mL,所以乘以4.
(2)根据化合价升降法即可配平化学方程式;
(3)氧化还原反应的计算原则是电子得失总数相等,得出KMnO4与Fe2+的对应关系,由KMnO4求出Fe2+的量,因为样品配成了100mL溶液,滴定时取用了25.00mL,所以乘以4.
解答:解:(1)加入KOH后,溶液B含有KAlO2,而最后产物为明矾,所以X为H2SO4(或KHSO4),故答案为:H2SO4(或KHSO4);
(2)Mn元素的化合价由+7价降低到+2价,降低5价;S元素的化合价由+4价升高到+6价,升高了2价,最小公倍数为10,然后用观察法配平其它系数,
故答案为:2;5;2;2;5;4;
(3)①高锰酸钾具有强氧化性,能氧化橡胶管,只能盛放在酸式滴定管中.故答案为:酸式滴定管;
②根据电子守恒可知:KMnO4→5Fe2+,20.0g样品中含铁:0.025L×0.1mol/L×5×4×56g/mol=2.8g,则该产品中铁元素的质量分数为
×100%=14%,故答案为:14%.
(2)Mn元素的化合价由+7价降低到+2价,降低5价;S元素的化合价由+4价升高到+6价,升高了2价,最小公倍数为10,然后用观察法配平其它系数,
故答案为:2;5;2;2;5;4;
(3)①高锰酸钾具有强氧化性,能氧化橡胶管,只能盛放在酸式滴定管中.故答案为:酸式滴定管;
②根据电子守恒可知:KMnO4→5Fe2+,20.0g样品中含铁:0.025L×0.1mol/L×5×4×56g/mol=2.8g,则该产品中铁元素的质量分数为
| 2.8g |
| 20g |
点评:本题考查了流程图分析、离子方程式的配平、滴定及化学计算,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目