题目内容
【题目】高炉炼铁过程中发生的主要反应为 ![]() Fe2O3(s)+CO(g)=
Fe2O3(s)+CO(g)= ![]() Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K= , △H0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡.求该时间范围内反应的平均反应速率v(CO2)=、CO的平衡转化率=:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是 .
A.减少Fe的量
B.增加Fe203的量
C.移出部分CO2
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂.
【答案】
(1)![]() ;<
;<
(2)0.006mol/(L?min);60%
(3)C
【解析】解:(1)由平衡常数是指在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值,但需要注意但是固体和纯液体的浓度视为常数,不能出现在表达式中,则K= ![]() ,又从表中数据可知随着温度的升高平衡常数逐渐减小,则说明温度升高平衡向逆反应方向移动,所以正反应是放热反应,即△H<0,所以答案是:
,又从表中数据可知随着温度的升高平衡常数逐渐减小,则说明温度升高平衡向逆反应方向移动,所以正反应是放热反应,即△H<0,所以答案是: ![]() ;<;(2)设CO转化的物质的量为x,则
;<;(2)设CO转化的物质的量为x,则
| CO(g) | ═ |
| CO2(g) | |
起始量(mol) | 1.0 | 1.0 | |||
转化的量(mol) | x | x | |||
平衡时的量(mol) | 1.0﹣x | 1.0+x |
又在1000℃时K=4.0,则有 ![]() =4.0,解得x=0.6, CO2的浓度变化量为:c(CO2)=
=4.0,解得x=0.6, CO2的浓度变化量为:c(CO2)= ![]() =0.06mol/L,则用二氧化碳表示的反应速率为
=0.06mol/L,则用二氧化碳表示的反应速率为 ![]() =0.006mol/(L.min),CO的转化率为
=0.006mol/(L.min),CO的转化率为 ![]() ×100%=60%,所以答案是:0.006mol/(L.min);60%;(3)若提高CO的平衡转化率,则化学平衡向正反应方向移动,因Fe、Fe2O3都是固体,改变质量平衡不移动,故AB不选;移出二氧化碳气体,减小生成物中气体的浓度,则平衡正向移动,故C选;因反应为放热反应,则升高温度,平衡向逆反应方向移动,故D不选;因该反应前后气体的体积不变,则减小容器的容积,平衡不移动,故E不选;因催化剂对平衡移动无影响,则加入合适的催化剂不能使平衡移动,故F不选;所以答案是:C.
×100%=60%,所以答案是:0.006mol/(L.min);60%;(3)若提高CO的平衡转化率,则化学平衡向正反应方向移动,因Fe、Fe2O3都是固体,改变质量平衡不移动,故AB不选;移出二氧化碳气体,减小生成物中气体的浓度,则平衡正向移动,故C选;因反应为放热反应,则升高温度,平衡向逆反应方向移动,故D不选;因该反应前后气体的体积不变,则减小容器的容积,平衡不移动,故E不选;因催化剂对平衡移动无影响,则加入合适的催化剂不能使平衡移动,故F不选;所以答案是:C.
【考点精析】掌握反应速率的定量表示方法和化学平衡状态本质及特征是解答本题的根本,需要知道反应速率的单位:mol/(L·min)或mol/(L·s) v=△c-△t;化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).

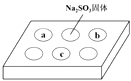
【题目】某同学进行SO2的性质实验。在点滴板a、b、c处分别滴有不同的试剂,再向Na2SO3固体上滴加数滴浓H2SO4后,在整个点滴板上盖上培养皿,一段时间后观察到的实验现象如下表所示。( )
序号 | 试剂 | 实验现象 |
|
a | 品红溶液 | 红色褪去 | |
b | 酸性KMnO4溶液 | 紫色褪去 | |
c | NaOH溶液(含2滴酚酞) | 红色褪去 |
下列说法正确的是
A.浓硫酸与Na2SO3固体发生了氧化还原反应
B.a、b均表明SO2具有漂白性
C.c中只可能发生反应:SO2+ 2OH—= SO32-+ H2O
D.c中所得溶液的离子浓度一定存在关系:c(Na+)+c(H+) = 2c(SO32-) +c(HSO3) + c(OH)
【题目】近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现在实验室中模拟甲醇合成反应,在2 L密闭容器内,400 ℃时发生反应:CO(g)+2H2(g)![]() CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 5 |
n(CH3OH) (mol) | 0 | 0.009 | 0.012 | 0.013 | 0.013 |
(1)下图中表示CH3OH的浓度变化的曲线是_________(填字母)。

(2)用H2表示从0~2s内该反应的平均速率v(H2) =__________。随着反应的进行,该反应的速率在逐渐减慢的原因是 _____________。
(3)能说明该反应已达到平衡状态的是________。
a.容器内CO与CH3OH的浓度相等 b.v逆(CO) = v正(H2)
c.容器内气体的密度保持不变 d.容器内气体的压强不变
(4)该反应是一个放热反应,说明该反应中破坏1mol CO和2mol H2的化学键吸收的能量_________形成1mol CH3OH释放的能量(填“﹤”、“=”或“﹥”)。
(5)已知在400 ℃时,反应CO(g)+2H2(g)![]() CH3OH(g) 生成1 mol CH3OH(g),放出的热量为116 kJ。计算上述反应达到平衡时放出的热量Q =_________kJ。
CH3OH(g) 生成1 mol CH3OH(g),放出的热量为116 kJ。计算上述反应达到平衡时放出的热量Q =_________kJ。