题目内容
12.设NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 在常温常压下,11.2 L Cl2含有的分子数为0.5NA | |
| B. | 在常温常压下,1 mol氢气含有的分子数为NA | |
| C. | 在常温常压下,32 g氧气含原子数为NA | |
| D. | 标准状况下,1mol水的体积约为22.4L |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、根据分子个数N=nNA来计算;
C、氧气由氧原子构成;
D、标况下,水为液态.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氯气的物质的量小于0.5mol,则分子个数小于0.5NA个,故A错误;
B、1mol氢气中含有的氢气分子个数N=nNA=NA个,故B正确;
C、氧气由氧原子构成,故32g氧气中含有的氧原子的个数N=$\frac{32g}{16g/mol}×{N}_{A}$=2NA,故C错误;
D、标况下,水为液态,1mol水的体积小于22.4L,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
2.将20克NaOH溶于水中,配制成1L溶液,则该溶液的物质的量浓度为( )
(已知NaOH的摩尔质量为40g/mol)
(已知NaOH的摩尔质量为40g/mol)
| A. | 0.1mol/L | B. | 0.5mol/L | C. | 4mol/L | D. | 1mol/L |
20.已知有反应BrO${\;}_{3}^{-}$+5Br-+6H+═3Br2+3H2O.下列反应中从反应原理来看与该反应最相似的是( )
| A. | 2KNO3═2KNO2+O2↑ | B. | NH4HCO3═NH3↑+CO2↑+H2O | ||
| C. | 3NO2+H2O═2HNO3+NO | D. | SO2+2H2S═3S↓+2H2O |
7.一定温度下,反应N2(g)+3H2(g)?2NH3(g)达到化学平衡状态的标志是( )
| A. | 断开1 mol H-H的同时断开2 mol N-H | |
| B. | c(N2):c(H2):c(NH3)=1:3:2 | |
| C. | N2与H2的物质的量之和是NH3的物质的量2倍 | |
| D. | 单位时间里每增加1molN2,同时增加3molH2 |
17.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | HNO3 | B. | Cl2 | C. | SO2 | D. | NH4NO3 |
4.有关热化学方程式书写与对应表述均正确的是( )
| A. | 稀硫酸与0.1mol/LNaOH溶液反应:H+(aq)+OH-1(aq)═H2O(l)△H=-57.3kJ•mol-1 | |
| B. | 在101KPa下氢气的标准燃烧热△H=-285.5kJ•mol-1,则水分解的热化学方程式:2H2O(l)═2H2(g)+O2(g)△H=+285.5kJ•mol-1 | |
| C. | 已知2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1,则可知C的标准燃烧热为110.5kJ•mol-1 | |
| D. | 密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量,则Fe(s)+S(g)═FeS(s)△H=-95.6kJ•mol-1 |
1.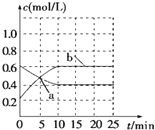 2NO2(g)?N2O4(g)△H<0.现将NO2和N2O4混合气体通入恒温密闭容器中,反应中物质浓度随时间的变化如图.下列说法正确的是( )
2NO2(g)?N2O4(g)△H<0.现将NO2和N2O4混合气体通入恒温密闭容器中,反应中物质浓度随时间的变化如图.下列说法正确的是( )
 2NO2(g)?N2O4(g)△H<0.现将NO2和N2O4混合气体通入恒温密闭容器中,反应中物质浓度随时间的变化如图.下列说法正确的是( )
2NO2(g)?N2O4(g)△H<0.现将NO2和N2O4混合气体通入恒温密闭容器中,反应中物质浓度随时间的变化如图.下列说法正确的是( )| A. | a点表示反应处于平衡状态 | |
| B. | 25 min末,若增大压强,化学平衡常数增大 | |
| C. | 25 min末,若升高温度,NO2的体积分数减小 | |
| D. | 10min内用N2O4表示的平均速率为0.02mol•L-1•min-1 |