题目内容
已知:CO(g) + H2O(g)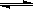 H2(g) + CO2(g)的平衡常数K随温度的变化如
H2(g) + CO2(g)的平衡常数K随温度的变化如
下表 ,下列说法正确的是
A.正反应是吸热反应
B.830℃时,反应达到平衡,[CO]=[CO2]
C.恒温时缩小容器体积使压强增大,正反应速率增大
D.400℃时,恒容反应器中投入CO、H2O、H2、CO2物质的量分别为5 mol、1 mol、2 mol、3mol,反应向逆方向进行
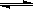 H2(g) + CO2(g)的平衡常数K随温度的变化如
H2(g) + CO2(g)的平衡常数K随温度的变化如下表 ,下列说法正确的是
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
A.正反应是吸热反应
B.830℃时,反应达到平衡,[CO]=[CO2]
C.恒温时缩小容器体积使压强增大,正反应速率增大
D.400℃时,恒容反应器中投入CO、H2O、H2、CO2物质的量分别为5 mol、1 mol、2 mol、3mol,反应向逆方向进行
C
A、温度升高,平衡常数减小,逆向移动,逆向吸热,正向放热;
B、达到平衡有[H2O][CO]=[H2][CO2];
C、压强增大,速率增大;
D、400℃,Q=1.2<K,故平衡正向移动
B、达到平衡有[H2O][CO]=[H2][CO2];
C、压强增大,速率增大;
D、400℃,Q=1.2<K,故平衡正向移动

练习册系列答案
相关题目
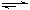 y C(g),如图表示在不同条件下反应物B的体积分数φ(B)随时间变化的关系,据此判断
y C(g),如图表示在不同条件下反应物B的体积分数φ(B)随时间变化的关系,据此判断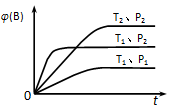
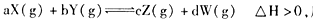 反应5min达到平衡时,X减小n mol·L-1,用Y表示的反应速率为0.6n mol·L-1·min-1。若将体系压强增大,W的百分含量不发生变化,则下列描述正确的是 ( )
反应5min达到平衡时,X减小n mol·L-1,用Y表示的反应速率为0.6n mol·L-1·min-1。若将体系压强增大,W的百分含量不发生变化,则下列描述正确的是 ( ) CO(g)+H2(g);②CO(g)+H2O(g)
CO(g)+H2(g);②CO(g)+H2O(g)  2NH3 ΔH<0。能使合成氨反应进行程度增大的方法是
2NH3 ΔH<0。能使合成氨反应进行程度增大的方法是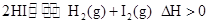 ,
, 的物质的量随时间的变化如图示,下列说法正确的是
的物质的量随时间的变化如图示,下列说法正确的是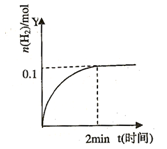
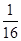
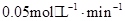
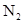 ,平衡不移动,反应速率不变
,平衡不移动,反应速率不变 H++OH—;△H>0,下列叙述正确的是
H++OH—;△H>0,下列叙述正确的是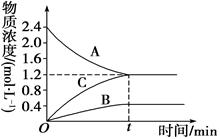
 容包括:化学平衡、电离平衡、水解平衡和
容包括:化学平衡、电离平衡、水解平衡和 4C(g) △H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)
4C(g) △H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)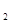 (g)
(g) 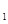 与K
与K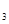 的平衡常数K=19。在该温度下的体积
的平衡常数K=19。在该温度下的体积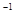 c0(O
c0(O
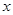 kJ·mol
kJ·mol +b>
+b>