题目内容
在一定温度下,向2L体积固定的密闭容器中加入lmolHI,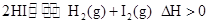 ,
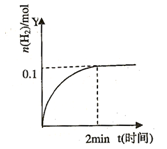
, 的物质的量随时间的变化如图示,下列说法正确的是
的物质的量随时间的变化如图示,下列说法正确的是
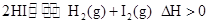 ,
, 的物质的量随时间的变化如图示,下列说法正确的是
的物质的量随时间的变化如图示,下列说法正确的是
A.该温度下,反应的平衡常数是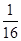 |
B.0~2min内的HI的平均反应速率为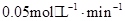 |
C.恒压下向该体系中加入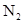 ,平衡不移动,反应速率不变 ,平衡不移动,反应速率不变 |
| D.升高温度,平衡向正反应方向移动,只有正反应速率加快 |
B
2HI  H2 + I2
H2 + I2
初n: 1mol 0 0
△n: 0.2mol 0.1mol 0.1mol
2min n:0.8mol 0.1mol 0.1mol
则该温度下的平衡常数为:K=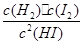 =
=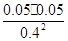 =
=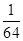
0~2min内的HI的平均反应速率为:υ(HI)=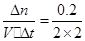 =
=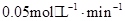
恒压下向该体系中加入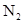 ,各反应混合物的浓度等倍减小,相当于减压,由于反应两边的气体系数相等,故平衡不移动,但正逆反应速率等倍数降低。
,各反应混合物的浓度等倍减小,相当于减压,由于反应两边的气体系数相等,故平衡不移动,但正逆反应速率等倍数降低。
升温时,正逆反应速率均增大,吸热反应的速率增加相对更大,平衡向吸热反应方向移动,即正向移动。
故答案为B
 H2 + I2
H2 + I2初n: 1mol 0 0
△n: 0.2mol 0.1mol 0.1mol
2min n:0.8mol 0.1mol 0.1mol
则该温度下的平衡常数为:K=
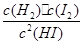 =
=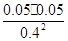 =
=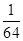
0~2min内的HI的平均反应速率为:υ(HI)=
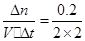 =
=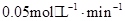
恒压下向该体系中加入
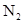 ,各反应混合物的浓度等倍减小,相当于减压,由于反应两边的气体系数相等,故平衡不移动,但正逆反应速率等倍数降低。
,各反应混合物的浓度等倍减小,相当于减压,由于反应两边的气体系数相等,故平衡不移动,但正逆反应速率等倍数降低。升温时,正逆反应速率均增大,吸热反应的速率增加相对更大,平衡向吸热反应方向移动,即正向移动。
故答案为B

练习册系列答案
相关题目
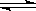 2E(g),若开始时只充入2 mol E(g),达平衡时,E的转化率为40%;若开始时充入2 mol M和1 mol N的混合气体,达平衡时混合气体的压强比起始时减少了
2E(g),若开始时只充入2 mol E(g),达平衡时,E的转化率为40%;若开始时充入2 mol M和1 mol N的混合气体,达平衡时混合气体的压强比起始时减少了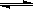 H2(g) + CO2(g)的平衡常数K随温度的变化如
H2(g) + CO2(g)的平衡常数K随温度的变化如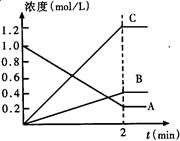
 2B(g)+C(g) △H>0,要使逆反应速率增大,A的浓度减小(只改变一个条件),应采取的措施是( )
2B(g)+C(g) △H>0,要使逆反应速率增大,A的浓度减小(只改变一个条件),应采取的措施是( ) 2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是
2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是 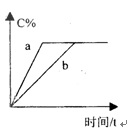
 3Y(g)+Z(g)达到平衡时,有30%的X发生分解,则平衡时混合气体总的物质的量是
3Y(g)+Z(g)达到平衡时,有30%的X发生分解,则平衡时混合气体总的物质的量是 N2O4达到平衡。(注意:视线b是一圆截面,颜色深浅可以看成有色分子在截面上的投影的密度大小)
N2O4达到平衡。(注意:视线b是一圆截面,颜色深浅可以看成有色分子在截面上的投影的密度大小)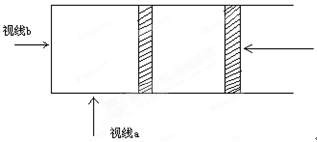
 2NO+O2,经过一定时间后,测得混合气中NO2浓度为0.06 mol·L-1, O2的浓度为0.12 mol·L-1,且各物质的浓度不再发生变化。
2NO+O2,经过一定时间后,测得混合气中NO2浓度为0.06 mol·L-1, O2的浓度为0.12 mol·L-1,且各物质的浓度不再发生变化。