题目内容
一定温度下,可逆反应2NO2(g)  2NO(g)+O2(g)在体积固定的密闭容器中反应,达到平衡状态的标志是 ( )
2NO(g)+O2(g)在体积固定的密闭容器中反应,达到平衡状态的标志是 ( )
①单位时间内生成n mol O2,同时生成2n mol NO2
②单位时间内生成n mol O2,同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1
④混合气体的压强不再改变
⑤混合气体的颜色不再改变
⑥混合气体的平均相对分子质量不再改变
 2NO(g)+O2(g)在体积固定的密闭容器中反应,达到平衡状态的标志是 ( )
2NO(g)+O2(g)在体积固定的密闭容器中反应,达到平衡状态的标志是 ( )①单位时间内生成n mol O2,同时生成2n mol NO2
②单位时间内生成n mol O2,同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1
④混合气体的压强不再改变
⑤混合气体的颜色不再改变
⑥混合气体的平均相对分子质量不再改变
| A.①④⑤⑥ | B.①②③⑤ | C.②③④⑥ | D.以上全部 |
A
①生成n mol O2,就是消耗2n mol NO2,即生成NO2的速率等于消耗NO2的速率,能表示v正=v逆,正确。②表示同一方向的反应速率,不能表示v正=v逆,不正确。③只要发生反应,或者说不论反应是否达到平衡,NO2、NO、O2的速率之比就为2∶2∶1,它不能反映可逆反应是否达到平衡,不正确。④温度、体积一定,混合气体压强不再改变,对于反应前后气体体积不相等的反应,说明气体的总物质的量不变,表明已达平衡。⑤颜色的深浅决定于有色物质NO2的浓度,混合气体颜色不变,说明NO2的浓度不再改变,能说明已达到平衡,正确。⑥混合气体的平均相对分子质量(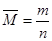 )不变,说明气体的总物质的量(n)不变,表明已达平衡,正确。
)不变,说明气体的总物质的量(n)不变,表明已达平衡,正确。
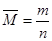 )不变,说明气体的总物质的量(n)不变,表明已达平衡,正确。
)不变,说明气体的总物质的量(n)不变,表明已达平衡,正确。
练习册系列答案
相关题目
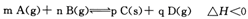 一段时间后达到化学平衡状态。改变某一条件,下列说法正确的是
一段时间后达到化学平衡状态。改变某一条件,下列说法正确的是 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下: Ni(CO)4(g)
Ni(CO)4(g)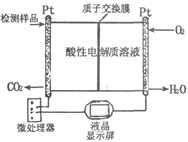
 +2H2O。
+2H2O。 CH3OH(g)+H2O(g)能判断该反应已达化学反应限度标志的是 (填字母)。
CH3OH(g)+H2O(g)能判断该反应已达化学反应限度标志的是 (填字母)。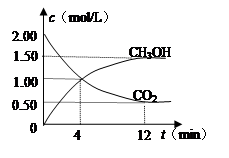
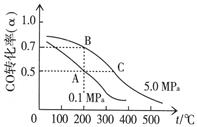
 CH3OH(g);已知密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率(α)与温度、压强的关系如右上图所示。
CH3OH(g);已知密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率(α)与温度、压强的关系如右上图所示。 pC(气) + qD(气)的 C %与时间 t有如图关系
pC(气) + qD(气)的 C %与时间 t有如图关系
 NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来 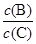 将 (填“增大”、“减小”或“不变”)。
将 (填“增大”、“减小”或“不变”)。