题目内容
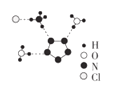
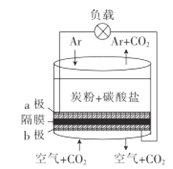
【题目】以熔融的碳酸盐(K2CO3)为电解液,泡沫镍为电极,氧化纤维布为隔膜(仅允许阴离子通过)可构成直接碳燃料电池,其结构如图所示,下列说法正确的是
A.该电池工作时,CO32-通过隔膜移动到a极
B.若a极通入空气,负载通过的电流将增大
C.b极的电极反应式为2CO2+O2-4e- =2CO32-
D.为使电池持续工作,理论上需要补充K2CO3
【答案】A
【解析】
A. 该电池的总反应方程式为:C+O2=CO2,炭粉在负(a)极失电子发生氧化反应,空气中的氧气在正(b)极得电子,该电池工作时,阴离子CO32-通过隔膜移动到a极,故A正确;
B. a极通入Ar,可以使炭粉和熔融碳酸盐的混合物隔绝空气,防止炭粉被氧化,如果a极通入空气,炭粉将直接被氧化,负载上没有电流通过,故B错误;
C. b极为正极,得电子发生还原反应,电极反应式为:2CO2+O2+4e- =2CO32-,故C错误;
D. 该电池的总反应方程式为:C+O2=CO2,从方程式可以看出钾离子和碳酸根离子都没有被消耗,因此理论上不需要补充K2CO3,故D错误;
故选A。

【题目】以磷石膏(只要成分CaSO4,杂质SiO2、Al2O3等)为原料可制备轻质CaCO3。
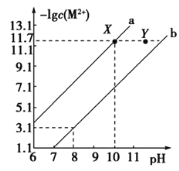
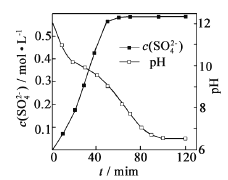
(1)匀速向浆料中通入CO2,浆料清液的pH和c(SO42-)随时间变化见由右图。清液pH>11时CaSO4转化的离子方程式_____________;能提高其转化速率的措施有____(填序号)
A.搅拌浆料 | B.加热浆料至100℃ |
C.增大氨水浓度 | D.减小CO2通入速率 |
(2)当清液pH接近6.5时,过滤并洗涤固体。滤液中物质的量浓度最大的两种阴离子为______和________(填化学式);检验洗涤是否完全的方法是_________。
(3)在敞口容器中,用NH4Cl溶液浸取高温煅烧的固体,随着浸取液温度上升,溶液中c(Ca2+)增大的原因___________。