题目内容
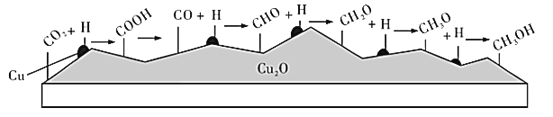
【题目】我国科学家在绿色化学领域取得新进展。利用双催化剂Cu和Cu2O,在水溶液中用H将CO2高效还原为重要工业原料之一的甲醇,其反应机理如图所示。则下列有关说法不正确的是( )
A.CO2生成甲醇是通过多步氧化反应实现的
B.该催化反应过程中涉及了化学键的形成及断裂
C.有可能通过调节控制反应条件获得甲醛等有机物
D.催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒
【答案】A
【解析】
A. CO2生成COOH,为还原反应;CO生成CHO,为还原反应;CHO生成CH2O,为还原反应;CH2O生成CH3O,为还原反应;CH3O生成CH3OH,为还原反应,所以CO2生成甲醇是通过多步还原反应实现,A错误;
B. 该催化过程发生化学反应,所以该反应中有化学键的形成和断裂,B正确;
C. CHO和H生成CH2O,需要Cu2O作催化剂,可以调节控制反应条件获得甲醛等有机物,C正确;
D.根据图知,催化剂Cu结合H原子,催化剂Cu2O结合含CHO微粒,催化剂Cu结合氢原子,催化剂Cu2O结合含碳微粒,D正确;
答案为A。

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案【题目】某温度下,在2L容器中3种物质间进行反应,X,Y,Z的物质的量随时间的变化曲线如图,反应在t1 min时到达平衡,如图所示:
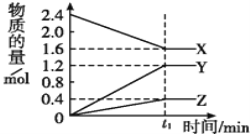
(1)该反应的化学方程式是_________。若t1=10min,用X表示化学反应速率为_________
(2)若上述反应中X,Y,Z分别为NH3、H2、N2, 且已知1mol氨气分解成氮气和氢气要吸收46kJ的热量,则至t1 min时,该反应吸收的热量为_______;
(3)保持容器温度不变,缩小容器体积,化学反应速率_______(填“增大”或“减小”或“不变”)。化学平衡常数K_______ (填“增大”或“减小”或“不变”)
(4)在一定容积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应的化学平衡常数表达式为K=__________
②能判断该反应达到化学平衡状态的依据是_______
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(5)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为__________℃;
(6)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2mol·L-1,c(H2)=1.5mol·L-1,c(CO)=1mol·L-1,c(H2O)=3mol·L-1,则下一时刻,反应向__________(填"正反应"或"逆反应")方向进行。