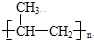题目内容
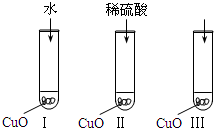 (2007?汕头二模)氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.
(2007?汕头二模)氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.(1)提出假设:假设 l:H2O能使氧化铜溶解
假设 2:
H+能够使CuO溶解
H+能够使CuO溶解
假设 3:SO42-能使氧化铜溶解
(2)通过实验Ⅰ可以证明假设
1
1
(填1、2、3)不成立;(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步所做的实验操作是:在Ⅲ中先加入
Na2SO4(或K2SO4等)
Na2SO4(或K2SO4等)
,再加入稀硫酸
稀硫酸
.(4)探究结果为
氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O、SO42-两种粒子都不能使CuO溶解
氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O、SO42-两种粒子都不能使CuO溶解
.你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是硝酸或盐酸等
硝酸或盐酸等
.分析:根据稀硫酸溶液中存在的微粒进行假设,确定实验步骤;通过对比实验确定起作用的微粒.
解答:解:(1)根据稀硫酸溶液中存在的微粒进行假设,溶液中存在H2O,H+,SO42-三种微粒,所以设计三个实验分别验证起作用的微粒,故答案为:H+能够使CuO溶解;
(2)Ⅰ中液体的成分是水,所以验证的是假设1,故答案为:1;
(3)要想证明起作用的是H+,首先要排除SO42-的嫌疑,所以在Ⅲ中先加入含SO42-的盐,然后再加入稀硫酸,故答案为:Na2SO4(或K2SO4等);稀硫酸;
(4)通过对比实验验证起作用的成分,得出结论是:氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O、SO42-两种粒子都不能使CuO溶解;氧化铜是金属氧化物,
能和酸反应生成盐和水,所以还可用盐酸和硝酸等来溶解氧化铜,故答案为;氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O、SO42-两种粒子都不能使CuO溶解;
盐酸和硝酸等.
(2)Ⅰ中液体的成分是水,所以验证的是假设1,故答案为:1;
(3)要想证明起作用的是H+,首先要排除SO42-的嫌疑,所以在Ⅲ中先加入含SO42-的盐,然后再加入稀硫酸,故答案为:Na2SO4(或K2SO4等);稀硫酸;
(4)通过对比实验验证起作用的成分,得出结论是:氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O、SO42-两种粒子都不能使CuO溶解;氧化铜是金属氧化物,
能和酸反应生成盐和水,所以还可用盐酸和硝酸等来溶解氧化铜,故答案为;氧化铜固体溶于稀H2SO4是稀硫酸H+在起作用,而H2O、SO42-两种粒子都不能使CuO溶解;
盐酸和硝酸等.
点评:本题考查的是性质实验的设计,性质探索性实验方案设计:从物质的结构特点去推测物质可能具有的性质,然后据此设计出合理的实验方案,去探索它可能具有的性质.我们推测的性质不一定准确,所以进行实验时要注意分析实验现象,从而得出正确结论.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
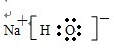

 (2007?汕头二模)2012年6月16日我国成功发射了“神州九号”.这标志着中国人的太空时代又前进了一大步.发射“神九”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气.已知:
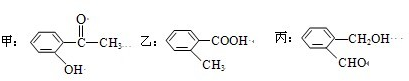
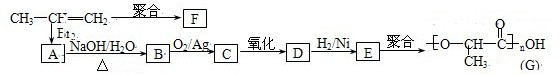
(2007?汕头二模)2012年6月16日我国成功发射了“神州九号”.这标志着中国人的太空时代又前进了一大步.发射“神九”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气.已知: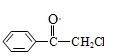 ,则苯氯乙酮不可能具有的化学性质是
,则苯氯乙酮不可能具有的化学性质是