题目内容
3.下列叙述正确的是( )①氧化还原反应的实质是元素的化合价发生改变
②若1mol气体的体积为22.4L,则它一定处于标准状况下
③标准状况下,1L HCl和1L H2O的物质的量相同
④在熔融状态下可以导电的物质就是电解质
⑤利用丁达尔现象区别溶液和胶体
⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑦在同温同体积时,气体物质的物质的量越大,则压强越大
⑧同温同压下,气体的密度与气体的相对分子质量成正比.
| A. | 除③外 | B. | ④⑤⑥⑦⑧ | C. | ⑤⑦⑧ | D. | ①⑤⑦⑧ |
分析 ①氧化还原反应的实质是电子的转移;
②气体的体积取决于温度、压强,不一定标准状况下才是22.4L/mol;
③标准状况下,H2O为液体;
④在熔融状态下可以导电的物质也可为金属;
⑤胶体具有丁达尔现象;
⑥只有气体符合;
⑦根据PV=nRT判断;
⑧根据ρ=$\frac{m}{V}$=$\frac{nM}{n{V}_{m}}$判断.
解答 解:①氧化还原反应的实质是电子的转移,化合价的升降为特征,故错误;
②气体的体积取决于温度、压强,温度越高,压强越小,则体积越大,不一定标准状况下才是22.4L/mol,故错误;
③标准状况下,H2O为液体,故错误;
④在熔融状态下可以导电的物质也可为金属,不一定为电解质,故错误;
⑤胶体具有丁达尔现象,可鉴别,故正确;
⑥只有气体符合,故错误;
⑦由PV=nRT可知,在同温同体积时,气体物质的物质的量越大,则压强越大,故正确;
⑧由ρ=$\frac{m}{V}$=$\frac{nM}{n{V}_{m}}$可知同温同压下,气体的密度与气体的相对分子质量成正比,故正确.
故选C.
点评 本题考查较为综合,涉及氧化还原反应、电解质、阿伏伽德罗定律等知识,为高频考点,侧重于学生的分析能力的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
16.正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.
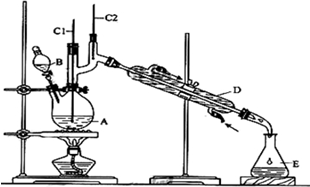
发生的反应如下:
CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{2}}$CH3CH2CH2CHO
反应物和产物的相关数据如下:
实验步骤如下:
①将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.
②在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分.
③将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.
回答下列问题:
(1)B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(2)沸石的作用是防止暴沸.
(3)将正丁醛粗产品置于分液漏斗中分液时,水在下层(填“上”或“下”)
(4)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(5)本实验中,正丁醛的产率为51%.

发生的反应如下:
CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{2}}$CH3CH2CH2CHO
反应物和产物的相关数据如下:
| 沸点/℃ | 密度(g.cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.5 | 0.8107 | 微溶 |
①将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.
②在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分.
③将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.
回答下列问题:
(1)B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(2)沸石的作用是防止暴沸.
(3)将正丁醛粗产品置于分液漏斗中分液时,水在下层(填“上”或“下”)
(4)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(5)本实验中,正丁醛的产率为51%.
8.分类方法在化学学科的发展中起到了非常重要的作用.下列分类标准合理的是( )
| A. | 根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等 | |
| B. | 根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液 | |
| D. | 根据氧化物中是否含有金属元素将氧化物分为酸性氧化物和碱性氧化物 |
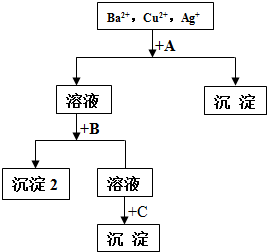 某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如图(写出最佳答案)
某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如图(写出最佳答案) 如图是中学实验中常用到的仪器.
如图是中学实验中常用到的仪器.
 爆鸣声和火花;然后过滤、洗涤、干燥;最后称量、计算,测得其产率只有预期值的63%左右。
爆鸣声和火花;然后过滤、洗涤、干燥;最后称量、计算,测得其产率只有预期值的63%左右。