题目内容
【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。回答下列问题:
(1)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度323K,NaClO2溶液浓度为5×10-3molL-1。反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO | SO | NO | NO | Cl- |
c/(molL-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式___。增加压强,NO的转化率___(填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐___ (填“增大”、“不变”或“减小”)。
③由实验结果可知,脱硫反应速率脱硝反应速率___ (填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___。
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中SO2和NO的平衡分压pc如图所示。

①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均___ (填“增大”、“不变”或“减小”)。
②反应ClO![]() +2SO
+2SO![]() =2SO
=2SO![]() +Cl-的平衡常数K表达式为___。
+Cl-的平衡常数K表达式为___。
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是___。
【答案】4NO+3ClO![]() +4OH-=4NO
+4OH-=4NO![]() +2H2O+3Cl- 提高 减小 大于 NO溶解度较低或脱硝反应活化能较高 减小
+2H2O+3Cl- 提高 减小 大于 NO溶解度较低或脱硝反应活化能较高 减小 ![]() 形成CaSO4沉淀,反应平衡向产物方向移动,SO2转化率提高
形成CaSO4沉淀,反应平衡向产物方向移动,SO2转化率提高
【解析】
(1)①NO、ClO2-在碱性条件下反应生成NO![]() 、Cl-,N元素化合价由+2价变为+5价、Cl元素化合价由+3价变为-1价,根据转移电子守恒及电荷守恒配平方程式为4NO+3ClO
、Cl-,N元素化合价由+2价变为+5价、Cl元素化合价由+3价变为-1价,根据转移电子守恒及电荷守恒配平方程式为4NO+3ClO![]() +4OH-=4NO
+4OH-=4NO![]() +2H2O+3Cl-;该反应前后气体体积减小,则增大压强平衡正向移动,NO的转化率提高;
+2H2O+3Cl-;该反应前后气体体积减小,则增大压强平衡正向移动,NO的转化率提高;
②根据脱硝反应方程式,以及可知,随着吸收反应的进行,氢氧根不断被消耗,溶液的pH减小,;
③由实验结果可知,在相同时间内硫酸根离子的浓度增加的多,因此脱硫反应速率大于脱硝反应速率;SO2较NO易溶于水,化学反应速率还与活化能有关,活化能越大化学反应速率越低,所以除了SO2和NO在烟气中的初始浓度不同,还可能是NO溶解度较低或脱硝反应活化能较高造成脱硝速率较慢;
(2)①由图分析可知,反应温度升高,SO2和NO的平衡分压pc增大,说明平衡逆向移动,脱硫、脱硝反应的平衡常数均减小;
②反应ClO![]() +2SO
+2SO![]() =2SO
=2SO![]() +Cl-的平衡常数
+Cl-的平衡常数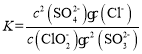 ;
;
(3)如果采用Ca(ClO)2替代NaClO2,生成硫酸钙沉淀,降低硫酸根离子浓度,促使平衡向正反应方向进行,所以Ca(ClO)2效果比次氯酸钠的效果好。

【题目】1,2-二氯丙烷(CH2C1CHClCH3)是一种重要的化工原料,工业上可用丙烯加成法制备,主要副产物为3-氯丙烯(CH2=CHCH2C1),反应原理为:
I.CH2=CHCH3(g)+C12(g)![]() CH2C1CHC1CH3(g) △H1=—134kJ·mol-1
CH2C1CHC1CH3(g) △H1=—134kJ·mol-1
II.CH2=CHCH3(g)+C12(g)![]() CH2=CHCH2C1(g)+HC1(g)△H2=—102kJ·mol-1
CH2=CHCH2C1(g)+HC1(g)△H2=—102kJ·mol-1
请回答下列问题:
(1)已知CH2=CHCH2C1(g)+HC1(g)![]() CH2C1CHC1CH3(g)的活化能Ea(正)为132kJ·mol-1,则该反应的活化能Ea(逆)为______kJ·mol-1。
CH2C1CHC1CH3(g)的活化能Ea(正)为132kJ·mol-1,则该反应的活化能Ea(逆)为______kJ·mol-1。
(2)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和C12(g)。在催化剂作用下发生反应I、Ⅱ,容器内气体的压强随时间的变化如下表所示。
时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
压强/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
①用单位时间内气体分压的变化来表示反应速率,即![]() ,则前120min内平均反应速率v(CH2C1CHC1CH3)=______kPa·min-1。(保留小数点后2位)。
,则前120min内平均反应速率v(CH2C1CHC1CH3)=______kPa·min-1。(保留小数点后2位)。
②该温度下,若平衡时HC1的体积分数为![]() ,则丙烯的平衡总转化率
,则丙烯的平衡总转化率![]() _______;反应I的平衡常数Kp=_____kPa-1(Kp为以分压表示的平衡常数,保留小数点后2位)。
_______;反应I的平衡常数Kp=_____kPa-1(Kp为以分压表示的平衡常数,保留小数点后2位)。
(3)某研究小组向密闭容器中充入一定量的CH2=CHCH3和C12,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得CH2C1CHC1CH3的产率与温度的关系如下图所示。
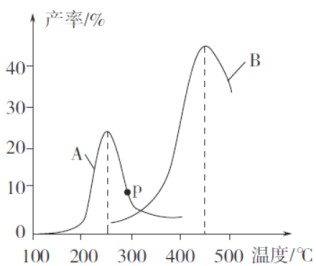
①下列说法错误的是___________(填代号)。
a.使用催化剂A的最佳温度约为250℃
b.相同条件下,改变压强不影响CH2C1CHC1CH3的产率
c.两种催化剂均能降低反应的活化能,但△H不变
d.提高CH2C1CHC1CH3反应选择性的关键因素是控制温度
②在催化剂A作用下,温度低于200℃时,CH2C1CHC1CH3的产率随温度升高变化不大,主要原因是_______________________________________________________________。
③p点是否为对应温度下CH2C1CHC1CH3的平衡产率,判断理由是_____________。