题目内容
某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液。若Cl2与KOH溶液反应时,被还原与被氧化的氯元素物质的量之比是11︰3,则混合液中ClO-与ClO3-的物质的量之比是( )
| A.1︰1 | B.1︰2 | C.1︰3 | D.2︰1 |
B
设混合液中ClO-与ClO3-的物质的量分别是x和y,则被还原的氯原子是11(x+y)/3,所以根据电子的得失守恒可知,11(x+y)/3=x+5y,解得x︰y=1︰2,选项B正确,答案选B。

练习册系列答案
相关题目
 2SO3,在一密闭容器中一定时间内达到平衡.
2SO3,在一密闭容器中一定时间内达到平衡.
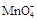 + —— Fe3++ Mn2++
+ —— Fe3++ Mn2++ 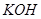 溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移
溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的混合溶液。若反应过程中转移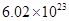 个电子,所得溶液中
个电子,所得溶液中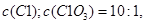 则参与反应的
则参与反应的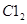 的物质的量为( )
的物质的量为( )