题目内容
(5分) (1)配平下列反应方程式并用双线桥标出电子转移的方向和数目
As2O3 + HNO3 + H2O = H3AsO4 + NO↑
(2)该反应中氧化剂是________,氧化产物是_________,当有1mol As2O3参加反应时转移电子的数目为
As2O3 + HNO3 + H2O = H3AsO4 + NO↑
(2)该反应中氧化剂是________,氧化产物是_________,当有1mol As2O3参加反应时转移电子的数目为
⑴
⑵HNO3 H3AsO4 4NA

⑵HNO3 H3AsO4 4NA
试题分析:⑴As2O3中As是+3价,H3AsO4中As是+5价;HNO3中N是+5价,NO中N是+2价。
(2)氧化剂是化合价升高、失去电子、被还原的物质;氧化产物是还原剂被氧化后生成的物质。
点评:苯题考查氧化还原反应,明确还原剂、氧化剂中元素的化合价变化是解答本题的关键,并熟悉用双线桥标出电子转移的方向和数目。

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目

 CuSO4+SO2↑+2H2O。试回答下列问题:
CuSO4+SO2↑+2H2O。试回答下列问题: ,
,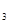 +H
+H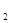 O
O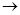 Al(OH)
Al(OH) 则生成标准状况下N
则生成标准状况下N