题目内容
X、Y、Z、W是原子序数依次递增的4种短周期元素。其中X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z原子的L层电子数比K层与M层电子数之和多5个,W在同周期元素中非金属性最强。下列说法正确的是( )
| A.X、Y、Z 3种元素组成的化合物中阴、阳离子所含电子数不等 |
| B.X与Z为同主族元素,它们的单质与W单质反应均失去电子 |
| C.Y、Z、W 3种元素组成的某种化合物可用于消毒 |
| D.Y与Z的单质在常温下反应生成Z2Y2 |
C
解析试题分析:X是周期表中原子半径最小的元素,则X是H;Y原子最外层电子数是次外层电子数的3倍,因此Y是O;Z原子的L层电子数比K层与M层电子数之和多5个,所以Z是Na;W在同周期元素中非金属性最强,且W的原子序数大于钠的,因此W是氯元素。H、O、Na种元素组成的化合物中氢氧化钠中阴、阳离子为OH?、Na+,所含电子数相等,都是10电子,故A项不正确;氢气和氯气化合生成氯化氢,形成的是共价键,通过共用电子对成键,B不正确;次氯酸钠可用于消毒,C正确;钠和氧气在常温下生成Na2O,D不正确。
考点:本题考查元素的推断、元素周期表的结构和元素周期律的应用。

 名校课堂系列答案
名校课堂系列答案短周期元素X、Y、Z和W的原子序数依次增大。X原子的S能级电子总数是P能级电子总数的2倍,Y与X同主族,Z和W原子中未成对电子数之比为2∶1。下列说法错误的是( )
| A.XW4为非极性分子 |
| B.Y、Z、W的最高价氧化物的水化物酸性强弱顺序是Y<Z<W |
| C.X、Y的氢化物由固态转化为气态时,克服相同的作用力 |
| D.XW4、YW4、ZW2分子中的中心原子均为sp杂化 |
下列物质与水反应最剧烈的是( )
| A.Rb | B.K | C.Na | D.Li |
下列各项内容中,排列顺序正确的是
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3 ②物质的熔点Li>Na>K
③微粒半径:K+>S2->F- ④单质的密度Na<K<Rb ⑤氢化物的沸点:H2Se>H2S>H2O
| A.①③ | B.②④ | C.①② | D.③⑤ |
已知元素周期表前三周期元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A.离子还原性Y2->Z- | B.质子数c>b |
| C.氢化物稳定性H2Y>HZ | D.原子半径X<W |
下列关于元素的叙述正确的是( )
| A.金属元素与非金属元素能形成共价化合物 |
| B.只有在原子中,质子数才与核外电子数相等 |
| C.目前使用的元素周期表中,最长的周期含有36种元素 |
| D.非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8 |
如图是元素周期表的一部分,下列关系正确的是
| S | Cl |
| Se | Br |
A.还原性:Se2->S2->C1- B.热稳定性:HC1>H2Se>HBr
C.原子半径:Se>C1>S D.酸性:HBrO4>HClO4>H2SO4
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是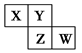
| A.元素W的最高价氧化物对应水化物的酸性最强 |
| B.单核阴离子半径的大小顺序为:r(W)>r(Y)>r(Z) |
| C.元素Y和元素Z的氢化物中均只存在极性共价键 |
| D.元素Y和元素Z的最高正化合价相同 |
短周期主族元素X、Y、Z、W的原子序数依次增大,元素X的原子半径最小,Y元素和X元素在一定条件下能形成YX,Z和W的原子序数相差8,W原子的电子总数是其电子层数的5倍。下列叙述正确的是( )
| A.Y可用于制造高性能可充电电池 |
| B.WX3的沸点高于ZX3 |
| C.Z的最高价含氧酸的酸性强于W的最高价含氧酸的酸性 |
| D.原子半径的大小顺序:rW>rZ>rY>rX |