题目内容
4.下列说法不正确的是( )| A. | 晶体硅可用作制造太阳能电池和光导纤维 | |
| B. | 用饱和氯化铵溶液可以清洗金属表面的锈迹 | |
| C. | “地沟油”禁止食用,但可用来制生物柴油和肥皂 | |
| D. | 高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 |
分析 A.光导纤维主要成分是二氧化硅;
B.氯化铵为强酸弱碱盐,水解显酸性;
C.地沟油是对生活中存在的各类劣质油的统称,长期食用可能会引发癌症,对人体的危害极大.其主要成分仍然是高级脂肪酸甘油酯,经加工处理后,可用来制肥皂和生物柴油,可以实现厨余废物合理利用;
D.铝合金具有质量轻,强度大,抗腐蚀能力比较强的优点.
解答 解:A.晶体硅可用作制造太阳能电池,不能制造光导纤维,故A错误;
B.饱和氯化铵溶液中铵根离子水解显酸性,能溶解金属氧化物,所以用饱和氯化铵溶液可以清洗金属表面的锈迹,故B正确;
C.地沟油属于油脂,油脂可发生皂化反应制肥皂;生物柴油是以动植物油脂、废餐饮用油等为原料与甲醇在催化剂作用下,进行酯交换制成的液体燃料,故C正确;
D.铝常温下能与空气中氧气反应,生成一层致密的氧化物保护膜,从而具有抗腐蚀性,铝合金材料的密度小,用以减轻列车质量,铝合金强度大,所以高铁车厢大部分材料采用铝合金,故D正确;
故选:A.
点评 本题为综合题,考查了材料的使用,盐类的水解,硅、油脂的性质及用途,熟悉相关物质的性质是解题关键,注意硅与二氧化硅用途的区别,为高考频考点,题目难度不大.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
14.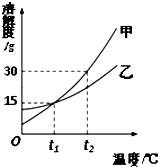 甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
 甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 将甲的饱和溶液变为不饱和溶液可采用降温的方法 | |
| C. | t1℃时,甲、乙的饱和溶液中溶质的质量分数不一定相等 | |
| D. | t2℃时,将甲、乙等质量的饱和溶液降温至t1℃,甲析出的固体一定大于乙 |
15.下列实验设计不合理的是( )
| A. | 比较相同条件下水解能力:室温下用pH计分别测量同浓度的Na2CO3和NaHCO3溶液的pH | |
| B. | 检验乙烯:无水乙醇和浓硫酸共热到170℃,将制得的气体通入酸性高锰酸钾溶液,观察到溶液紫色很快褪去,证明反应生成了乙烯 | |
| C. | 检验铝热剂中铁的价态:将铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,证明该铝热剂不含氧化铁 | |
| D. | 在2mL同浓度的NaCl、NaI混合溶液中滴入几滴稀AgNO3溶液,观察到产生黄色沉淀,证明Ksp(AgCl)>Ksp(AgI) |
12.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,用化学沉降法处理含砷废水,相关数据如下表.
回答以下问题:
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=0.2mol•L-1.
(2)写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]=c3(Ca2+)•c2(AsO43-),若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol•L-1,c(AsO43-)的最大是7.2×10-17mol•L-1.
(3)工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式2H++MnO2+H3AsO3=H3AsO4+Mn2++H2O.
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降.
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为CaSO4;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为H3AsO4是弱酸,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀.
| 表1.几种砷酸盐的Ksp | |
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-9 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 7.2×10-21 |
| 表2.工厂污染物排放浓度及允许排放标准 | ||
| 污染物 | H2SO4 | As |
| 浓度 | 19.6g/L | 1.6g•L-1 |
| 排放标准 | pH6~9 | 0.5mg•L-1 |
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=0.2mol•L-1.
(2)写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]=c3(Ca2+)•c2(AsO43-),若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol•L-1,c(AsO43-)的最大是7.2×10-17mol•L-1.
(3)工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式2H++MnO2+H3AsO3=H3AsO4+Mn2++H2O.
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降.
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为CaSO4;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为H3AsO4是弱酸,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀.
19.下列说法正确的是( )
| A. | 2NO2?N2O4-----①N2O4?2NO2--②,反应①的化学平衡常数是反应②的化学平衡常数的倒数 | |
| B. | 已知H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol将0.05mol/LBa(OH)2溶液100.0mL与0.05mol/LH2SO4溶液100.0mL混合,在298K101kPa条件下放热量为0.573kJ | |
| C. | 已知298K 时,0.10mol/L HAc的电离度为1.32%.在0.10mol/L HAc 和0.10mol/LNaAc的混合溶液20.00mL中,有如下变化: HAc?H++Ac----①,NaAc=Na++Ac-----②,Ac-+H2O?HAc+OH-----③,向该溶液中滴入几滴稀盐酸,溶液的pH保持相对稳定 | |
| D. | 将明矾与纯碱溶液混合,有沉淀产生,该沉淀的成分为碳酸铝 |
16.反应H2+C12=2HCl(△H<0)的机理包含:①C12→2C1(慢)②H2+Cl→HCl+H (快)③C12+H→HCl+Cl(快)等.下列说法不正确的是( )
| A. | 断开lmol H-H键需要的能量大于断开1mol Cl-Cl键需要的能量 | |
| B. | 反应H2+C12=2HCl在光照和加热条件下的△H不同 | |
| C. | 反应①的活化能大于反应②的活化能 | |
| D. | 已知反应②的△H>O,则反应③的△H一定小于0 |
13. M、X、Y、Z是四种常见的短周期元素,各元素在周期表中的位置如图所示,其中只有M属于金属元素.下列说法中,错误的是( )
M、X、Y、Z是四种常见的短周期元素,各元素在周期表中的位置如图所示,其中只有M属于金属元素.下列说法中,错误的是( )
 M、X、Y、Z是四种常见的短周期元素,各元素在周期表中的位置如图所示,其中只有M属于金属元素.下列说法中,错误的是( )
M、X、Y、Z是四种常见的短周期元素,各元素在周期表中的位置如图所示,其中只有M属于金属元素.下列说法中,错误的是( )| A. | X元素最高价氧化物对应水化物的酸性弱于Y元素的 | |
| B. | Y元素气态氢化物的稳定性大于Z元素的 | |
| C. | 元素Z在周期表中的位置为第2周期、VIA族 | |
| D. | M元素的氧化物既可以与强酸溶液反应,也可以与强碱溶液反应 |
14.铜和铜的化合物是重要的化工原料,常用作催化剂、防腐剂和消毒剂等制备合成.已知:CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):(见图1)

(1)配离子[Cu(En)2]2+的中心离子基态外围电子排布式为3d9;乙二胺分子中氮原子轨道的杂化类型为sp3;配离子[Cu(En)2]2+中的配位数为4;
(2)乙二胺和三甲胺[N(CH3)3]均属于胺类,但乙二胺比三甲胺的沸点高的多,原因是乙二胺分子之间可以形成氢键,三甲胺分子之间不能形成氢键;
(3)比较表中有大小(用“大于”或“小于”“等于”填空)
(4)氯和钾与不同价态的铜可形成两种化合物M和N,二都均可用于催化乙炔聚合,二者阴离子均为无限长链结构(见图2),下列分析正确的是BC.
A、图中a位置上Cl原子为sp杂化轨道;
B、M的化学式确认是KCuCl3,则N的化学式为K2CuCl3;
C、配离子[CuCl4]2-和配离子[AlCl4]-空间结构相似;
金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,反应的离子反应方程式为Cu+H2O2 +4NH3═Cu(NH3)42++2OH-;
(5)金属铁单质的晶体在不同温度下有两种堆积方式(晶胞分别如图3所示).已知体心立方与面心立方的晶胞堆积的空间利用率分别为68%和74%.列算式计算两种晶体的密度之比[ρ(a):ρ(b)]为3$\sqrt{3}$:4$\sqrt{2}$(化简成简单的关系式,不求计算结果,只填写结果不得分).

(1)配离子[Cu(En)2]2+的中心离子基态外围电子排布式为3d9;乙二胺分子中氮原子轨道的杂化类型为sp3;配离子[Cu(En)2]2+中的配位数为4;
(2)乙二胺和三甲胺[N(CH3)3]均属于胺类,但乙二胺比三甲胺的沸点高的多,原因是乙二胺分子之间可以形成氢键,三甲胺分子之间不能形成氢键;
(3)比较表中有大小(用“大于”或“小于”“等于”填空)
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| P>S | H->Li+ | KCl<Si | HClO3<HClO4 |
A、图中a位置上Cl原子为sp杂化轨道;
B、M的化学式确认是KCuCl3,则N的化学式为K2CuCl3;
C、配离子[CuCl4]2-和配离子[AlCl4]-空间结构相似;
金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,反应的离子反应方程式为Cu+H2O2 +4NH3═Cu(NH3)42++2OH-;
(5)金属铁单质的晶体在不同温度下有两种堆积方式(晶胞分别如图3所示).已知体心立方与面心立方的晶胞堆积的空间利用率分别为68%和74%.列算式计算两种晶体的密度之比[ρ(a):ρ(b)]为3$\sqrt{3}$:4$\sqrt{2}$(化简成简单的关系式,不求计算结果,只填写结果不得分).
 .
. .
.