题目内容
【题目】铝热反应有广泛的用途,实验装置如下图所示。
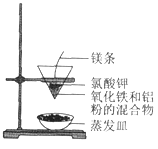
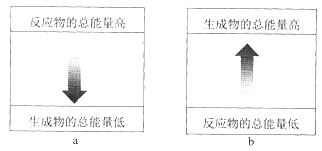
(1)铝热反应是 __________________(填“吸热”或“放热”)反应,其能量变化可用下图中的 ___________________(填序号)表示。
(2)该铝热反应的化学方程式是____________________________________。
(3)任写出铝热反应在实际生产中的一种用途____________________。
【答案】 放热 a 2Al+Fe2O3![]() Al2O3+2Fe 冶炼金属
Al2O3+2Fe 冶炼金属
【解析】(1)铝热反应是放热反应,反应物总能量高于生成物总能量,其能量变化可用a图表示。(2)该铝热反应的化学方程式是2Al+Fe2O3![]() Al2O3+2Fe。(3)铝热反应在实际生产中的用途可以是冶炼金属。
Al2O3+2Fe。(3)铝热反应在实际生产中的用途可以是冶炼金属。

【题目】下列说法正确的是( )
A.CH4与C4H10不一定是同系物
B.苯分子中既含有碳碳单键,又含有碳碳双键
C.乙烯使溴水褪色属于取代反应
D.炒菜时,加入一点酒和醋能使菜味香可口,原因是有酯类物质生成
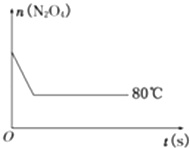
【题目】在80℃时,将0.40mol的N204气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O42NO2 , 隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
n(N2O4) | 0.40 | a | 0.20 | c | d | e |
n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)计算20s一40s内用N2O4表示的平均反应速率为molL﹣1S﹣1;
(2)计算在80℃时该反应的平衡常数K=(请注明单位).
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”.“变深”或“不变”)
(4)要增大该反应的K值,可采取的措施有(填序号):
A.增大N2O4的起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线.