��Ŀ����
����Ŀ��dz��ɫ��X��������Ԫ�أ������ᾧˮ��M(X)<908gmol-1��ijС��Ϊ��̽��X����ɺ����ʣ���Ʋ����������ʵ��
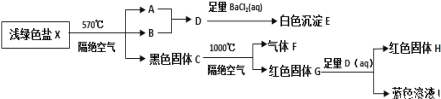
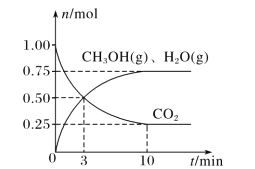
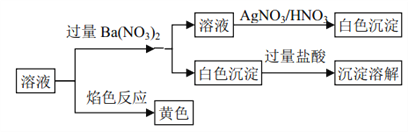
����ʵ���У��õ�23.3g��ɫ���� E��28.8g��ɫ����G��12.8g��ɫ����H��
��֪����X�ֽ��A��B��C�ķ�ӦΪ��������ԭ��Ӧ��
�ڳ�����B��Һ̬��1��B���Ӻ���10�����ӡ�
��ش��������⣺
(1)д��B���ӵĵ���ʽ_______________��X�Ļ�ѧʽ��__________��
(2)�ڸ���������570���¶��¼���X����ȫ�ֽ�Ļ�ѧ��Ӧ����ʽΪ��__________��
(3)��д��G����D��Һ�����ӷ���ʽ��_________________��
(4)�����ʵ��������C���Ƿ��Ժ���X��___________________��
���𰸡�![]() Cu4(OH)6SO4 Cu4(OH)6SO4
Cu4(OH)6SO4 Cu4(OH)6SO4![]() 4CuO+SO3��+3H2O�� Cu2O+2H+=Cu2++Cu+H2O ȡ������Ʒ���Թ��У���������ϡ�����ܽ⣬�ټ�������BaCl2��Һ����������ɫ��������Ʒ�к���X����֮��û�С�
4CuO+SO3��+3H2O�� Cu2O+2H+=Cu2++Cu+H2O ȡ������Ʒ���Թ��У���������ϡ�����ܽ⣬�ټ�������BaCl2��Һ����������ɫ��������Ʒ�к���X����֮��û�С�
��������
dz��ɫ��X��570�桢�����������������ȷֽ�Ϊ��������ԭ��Ӧ���õ�A��B�ͺ�ɫ����C��������B��Һ̬��1��B���Ӻ���10�����ӣ�BΪH2O��A��ˮ��Ӧ���ɵ�D�ܺ��Ȼ�����Ӧ���ɰ�ɫ����E��Eֻ��ΪBaSO4����DΪH2SO4��A��SO3��23.3g��ɫ����E�����ʵ���Ϊ0.1mol����ɫ����C����ΪFe3O4��CuO��C�ȣ���ɫ����C����������1000�淴Ӧ��������F�ͺ�ɫ����G��G�ܺ�H2SO4��Ӧ���ɺ�ɫ�������ɫ��ҺӦΪCu2O��������Һ�е��绯��Ӧ��Cu2O+H2SO4=Cu+CuSO4+H2O�����Ժ�ɫ����CΪCuO��GΪCu2O������FΪO2����ɫHΪCu����ɫ��ҺIΪCuSO4��Ȼ���Ϸ�Ӧ���������ʵ������������ʵ������������ʵ����ıȵ���ԭ�Ӹ����ȣ�����䲻���нᾧˮ��ȷ��X�Ļ�ѧʽ���������йؽ��
��������������֪A��SO3��B��H2O��C��CuO��D��H2SO4��E��BaSO4��F��O2��GΪCu2O��HΪCu��IΪCuSO4��X�Ǻ���Cu��H��O��S����Ԫ�صĻ����
(1)BΪH2O��ˮ������H��Oԭ��֮���Թ��ۼ���ϣ�����ʽΪ��![]() ������Ԫ���غ��֪����dz��ɫ��X��n(Cu)=2n(Cu2O)=2��
������Ԫ���غ��֪����dz��ɫ��X��n(Cu)=2n(Cu2O)=2��![]() =0.4mol��n(CuO)=0.4mol��n(S)=n(BaSO4)=
=0.4mol��n(CuO)=0.4mol��n(S)=n(BaSO4)=![]() =0.1mol��n(CuO)��n(SO3)=0.04mol��0.01mol=4��1����������Ԫ�أ������ᾧˮ���軯ѧʽΪ��Cu4(OH)mSO4��Cu4(OH)mSO4
=0.1mol��n(CuO)��n(SO3)=0.04mol��0.01mol=4��1����������Ԫ�أ������ᾧˮ���軯ѧʽΪ��Cu4(OH)mSO4��Cu4(OH)mSO4![]() 4CuO+SO3��+
4CuO+SO3��+![]() H2O����������Ԫ���غ�ã�m=6������M(X)<908g/mol������X��ѧʽΪCu4(OH)6SO4��
H2O����������Ԫ���غ�ã�m=6������M(X)<908g/mol������X��ѧʽΪCu4(OH)6SO4��
(2)X�ڸ���������570���¶��¼��ȷ���Cu4(OH)6SO4![]() 4CuO+SO3��+3H2O����
4CuO+SO3��+3H2O����
(3)ש��ɫ����G��Cu2O��������ϡH2SO4����������ԭ��Ӧ������Cu��CuSO4��H2O����Ӧ�����ӷ���ʽΪ��Cu2O+2H+=Cu+Cu2++H2O��
(4)��ɫ����CΪCuO���纬��X������ü���SO42-�ķ������飬�����ǣ�ȡ������Ʒ���Թ��У���������ϡ�����ܽ⣬�ټ��������Ȼ�����Һ����������ɫ����������Ʒ�к���X����֮��û�С�

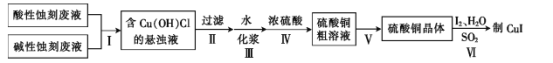
 ������������ϵ�д�
������������ϵ�д�����Ŀ����������(NaN3)��������ȫ��������������巢����ԭ�ϡ������ǹ�ҵˮ���·��Ʊ��������ƵĹ������̣�
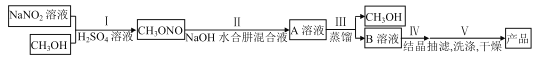
��֪ NaN3 ���� AgNO3 ��Ӧ���ɰ�ɫ������ˮ�� AgN3���й����ʵ��������������
���� | �۵�� | �е�� | �ܽ��� |
CH3OH | -97 | 64.7 | ��ˮ���� |
ˮ����(N2H4H2O) | 2 | 113.5 | ��ˮ�������ܣ����������Ѻ��ȷ� |
���������(CH3ONO) | -17 | -12 | �����Ҵ������� |
��������(NaN3) | 410(�ֽ�) | ���� | ������ˮ�������ڴ������������� |
��ش�
(1)�������NaNO2��ϡ���ᷢ������Ӧ����������������ӷ���ʽΪ��________�������������NaN3�Ļ�ѧ����ʽΪ��____________��
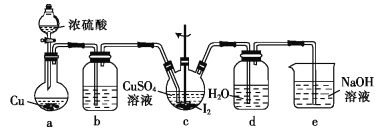
(2)ʵ����ģ�ⲽ��II ʵ��װ����ͼ(װ������ȴˮʡ�ԣ���ͬ)��
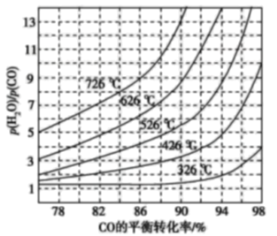
�ٸ���ʵ�鷢���¶���20�����ҷ�Ӧ��ѡ���Ժ�ת������ߣ����Ǹ÷�Ӧ���ڷ��ȷ�Ӧ����˿��Բ�ȡ�Ĵ�ʩ��_______________________��
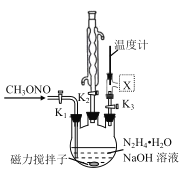
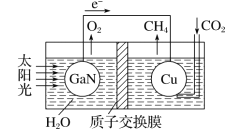
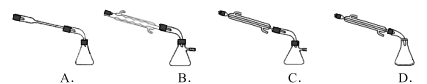
��ͼ��X�����ӵ������װ��ӦΪ��ͼ�е�______ ��
(3)���������Һ B ������������Һ�����![]() ��NaN3 �ᾧ������
��NaN3 �ᾧ������
�ٲ��������______________ϴ�Ӿ��塣
A.ˮ B.�Ҵ� C.�Ҵ�ˮ��Һ D.����
�ڳ����ζ����ⶨ��Ʒ���ȣ����Ե���ɫK2CrO4��Һ��ָʾ������AgNO3����Һ������Ʒ��Һ��������Ag2CrO4���֣�����Һ�ʵ���ɫΪ�յ㡣AgNO3��ҺҪװ����ɫ����ʽ�ζ�������еζ���������_________________________��
�����в������жϺ�������__________��
A���ζ��ܺ���Һ�ܹܼⲻ�ɽӴ���ƿ�ڱ�
B
C���ζ������п�������ˮ����ƿ����ճ������Һ����
D���ζ��յ�ʱ����δ�ȵζ���Һ���ȶ��Ͷ����ᵼ�²ⶨ���ƫ��