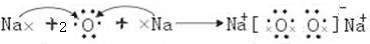题目内容
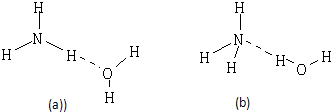
 (1)分别用电子式表示HClO、MgCl2的形成过程
(1)分别用电子式表示HClO、MgCl2的形成过程 、
、
 、
、
(2)已知下列原电池的总反应式:Cu+2FeCl3═CuCl2+2FeCl2,请写出电极反应式:
正极反应式为:
2Fe 3++2e -═2Fe 2+
2Fe 3++2e -═2Fe 2+
负极反应式为:
Cu-2e -═Cu 2+
Cu-2e -═Cu 2+
(3)如图所示,在锥形瓶放置有装有水的小试管,往小试管中分别加入下列物质时:①烧碱固体 ②浓硫酸 ③硝酸铵固体 ④NaCl固体,其中能使a端液面高于b端液面的是
③
③
.(填序号)分析:用电子式表示物质的形成过程时,左边的相同原子可以合并,右边相同原子或离子不能合并,中间用箭头连接;原电池中负极反应氧化反应正极反应还原反应;容器内温度升高,压强增大,反之压强减小,液体向压强小的方向移动.
解答:解:(1)左边写原子的电子式,相同原子可以合并,右边写物质的电子式,中间用箭头连接.HClO为共价化合物,用电子式表示的形成过程为 ,MgCl2为离子化合物,用电子式表示的形成过程为
,MgCl2为离子化合物,用电子式表示的形成过程为 ,
,
故答案为: ;
; ;
;
(2)铜失去电子发生氧化反应,是负极反应,电极反应为Cu-2e-═Cu2+,;铁离子得到电子发生还原反应是正极反应,电极反应为2Fe3++2e-═2Fe2+,
故答案为:正极:2Fe3++2e-═2Fe2+; 负极:Cu-2e-═Cu2+;
(3)a端高说明锥形瓶内气体压强降低,温度降低,则试管中的过程是吸热过程,而硝酸铵溶于水为吸热过程,
故答案为:③.
 ,MgCl2为离子化合物,用电子式表示的形成过程为
,MgCl2为离子化合物,用电子式表示的形成过程为 ,
,故答案为:
 ;
; ;
;(2)铜失去电子发生氧化反应,是负极反应,电极反应为Cu-2e-═Cu2+,;铁离子得到电子发生还原反应是正极反应,电极反应为2Fe3++2e-═2Fe2+,
故答案为:正极:2Fe3++2e-═2Fe2+; 负极:Cu-2e-═Cu2+;
(3)a端高说明锥形瓶内气体压强降低,温度降低,则试管中的过程是吸热过程,而硝酸铵溶于水为吸热过程,
故答案为:③.
点评:书写电子式时要根据原子实际的成键情况书写.本题中次氯酸电子式如果按照分子式的书写形式书写就错了

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
 ;
; .
.
 元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.

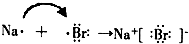
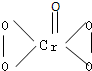 ?
?