题目内容
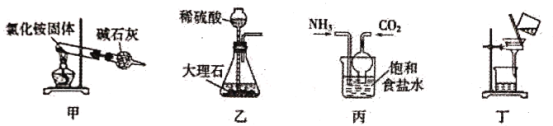
【题目】实验室制备溴乙烷(C2H5Br)的装置和步骤如下:(已知溴乙烷的沸点38.4℃)①检查装置的气密性,向装置图所示的∪形管和大烧杯中加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小心加热,使其充分反应.回答下列问题:

(1)该实验制取溴乙烷的化学方程式为:__.
(2)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为__,同时生成的无色气体分子式为__.
(3)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是__.
(4)U型管内可观察到的现象是__.
(5)反应结束后,∪形管中粗制的C2H5Br呈棕黄色.为了除去粗产品中的杂质,可选择下列试剂中的__(填序号).
(a)NaOH溶液 (b)H2O (c)Na2SO3溶液 (d)CCl4
所需的主要玻璃仪器是__(填仪器名称).要进一步制得纯净的C2H5Br,可用水洗,然后加入无水CaCl2,再进行__(填操作名称).
(6)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后__(填代号).
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却.
【答案】NaBr+H2SO4+C2H5OH![]() NaHSO4+C2H5Br+H2O Br2 SO2和H2O 水浴加热 有油状液体生成 c 分液漏斗 蒸馏 ④①⑤③②
NaHSO4+C2H5Br+H2O Br2 SO2和H2O 水浴加热 有油状液体生成 c 分液漏斗 蒸馏 ④①⑤③②
【解析】
(1)乙醇、浓硫酸和溴化钠加热反应生成溴乙烷、硫酸氢钠和水;
(2)浓硫酸具有强氧化性,温度过高会把溴离子氧化成红棕色的溴,同时浓硫酸被还原成二氧化硫;
(3)为了更好的控制温度,最好用水浴加热的方法;
(4)U型管得到了溴乙烷;
(5)溴乙烷中混有溴,除杂时注意溴和溴乙烷的性质角度考虑;分液用到分液漏斗;将溴乙烷与水分离采用蒸馏操作;
(6)检验溴乙烷中溴元素,应在碱性条件下水解,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成;有溴乙烷参加的主要反应是溴乙烷和碱溶液中的水解。
(1)溴化钠、浓硫酸和乙醇制取溴乙烷的化学方程式为:NaBr+H2SO4+C2H5OH![]() NaHSO4+C2H5Br+H2O,故答案为:NaBr+H2SO4+C2H5OH
NaHSO4+C2H5Br+H2O,故答案为:NaBr+H2SO4+C2H5OH![]() NaHSO4+C2H5Br+H2O;
NaHSO4+C2H5Br+H2O;
(2)由于浓硫酸具有强氧化性,会有溴生成,化学式为Br2,同时浓硫酸被还原成SO2,因此无色气体为SO2和H2O,故答案为:Br2;SO2和H2O;
(3)为了更好的控制温度,最好用水浴加热的方法,故答案为:水浴加热;
(4)U型管得到了溴乙烷,因此可观察到有油状液体生成,故答案为:有油状液体生成;
(5)粗制的C2H5Br呈棕黄色,说明含有单质溴杂质,则,
a.溴乙烷能够与氢氧化钠反应,故A错误;
b.溴在溴乙烷中的溶解度比在水中大,加水难以除去溴乙烷中的溴,故B错误;
c.Na2SO3与溴发生氧化还原反应,Na2SO3可除去溴,故C正确;
d.溴和溴乙烷都能溶于四氯化碳,不能将二者分离,故D错误;
分液使用的主要仪器是分液漏斗,要进一步制得纯净的C2H5Br,可用水洗,然后加入无水CaCl2,利用沸点不同再进行蒸馏分离,故答案为:c;分液漏斗;蒸馏;
(6)检验溴乙烷中溴元素,应在碱性条件下水解,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成,所以操作顺序为④①⑤③②,故答案为:④①⑤③②。

【题目】下表是五种主族元素的结构特点及其元素、单质、化合物的性质.
元素 | 结构特点及元素、单质、化合物的性质 |
X | 气态氢化物与最高价氧化物对应水化物可以化合成盐 |
Y | 原子中s电子数与p电子数相同,且p电子的能量最高 |
Z | 单质在空气中燃烧产生黄色火焰,生成黄色粉末 |
W | 最外层电子排布(n+1)sn(n+1)pn﹣1 |
T | 单质升华可以产生紫色的烟 |
(1)写出X元素的原子核外电子排布__;其单质的化学性质__(填“稳定”或“活泼”),该元素的非金属性__(填“强”或“弱”),证明其强弱的理由是__.
(2)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式__;已知w的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为__.
(3)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反 应的离子方程式:__,__.
(4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱.Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为__.
A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3.