题目内容
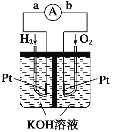
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
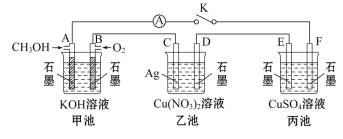
(1)甲池中A电极的电极反应式为________。
(2)丙池的总离子反应方程式为_________。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗标准状况下O2的体积为_____mL。
(4)一段时间后,断开电键K,下列物质能使乙池电解质溶液恢复到反应前浓度的是______(填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
【答案】CH3OH+8OH--6e- == CO32- +6H2O 2Cu2++2H2O![]() 4H++2Cu+O2↑ 560 A
4H++2Cu+O2↑ 560 A
【解析】
由图可知,当闭合该装置的电键K时,甲池为甲醇燃料电池,通入甲醇的为负极,电极反应为:2CH3OH+16OH--12e-=CO32-+12H2O,通入氧气的为正极,电极反应为:3O2+12e-+6H2O=12OH-,KOH为电解质溶液;乙池为电解池,C为阳极,电极反应为:Ag-e-=Ag+,D为阴极,电极反应为:Cu2++2e-=Cu;丙池为电解池,E为阳极,电极反应为:4OH--4e-=O2↑+2H2O,F为阴极,电极反应为:Cu2++2e-=Cu,据此进行分析解答。
(1)甲池为甲醇燃料电池,A为负极,电极反应为:CH3OH+8OH--6e- == CO32- +6H2O;
(2)丙池为电解池,E为阳极,电极反应为:4OH--4e-=O2↑+2H2O,F为阴极,电极反应为:Cu2++2e-=Cu,总离子反应方程式为:2Cu2++2H2O![]() 4H++2Cu+O2↑
4H++2Cu+O2↑
(3)甲池B极为正极,电极反应为:3O2+12e-+6H2O=12OH-,乙池中C为阳极,电极反应为:Ag-e-=Ag+,乙池中C极质量减轻10.8 g,n(Ag)=![]() =0.1mol,电子转移0.1mol,甲池中消耗氧气的物质的量为
=0.1mol,电子转移0.1mol,甲池中消耗氧气的物质的量为![]() ×0.1mol=0.025mol,消耗标准状况下O2的体积为0.025mol×22.4L/mol=0.56L=560mL;
×0.1mol=0.025mol,消耗标准状况下O2的体积为0.025mol×22.4L/mol=0.56L=560mL;
(4)乙池为电解硝酸铜,用金属银作阳极,阴极上铜离子得电子生成单质铜,溶液中铜离子减少,要让乙池电解质溶液恢复到反应前浓度,需要加入金属铜。