题目内容
12.某单烯烃氢化后得到的饱和烃是: ,该烯烃可能的结构有( )
,该烯烃可能的结构有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
分析 加成反应指有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物,根据加成原理采取逆推法还原C=C双键,烷烃分子中相邻碳原子上均带至少1个氢原子的碳原子间是对应烯存在C=C的位置.
解答 解:根据烯烃与H2加成反应的原理,推知该烷烃分子中相邻碳原子上均带1个氢原子的碳原子间是对应烯存在C=C的位置.该烷烃的碳链结构为 ,能形成双键位置有3个,该烯烃共有3种,故选C.
,能形成双键位置有3个,该烯烃共有3种,故选C.
点评 本题以加成反应为载体,考查同分异构体的书写,理解加成反应原理是解题的关键,采取逆推法还原C=C双键,注意分析分子结构是否对称,防止重写、漏写.

练习册系列答案
相关题目
2.下列各物质中,不能够按照 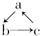 (“→”表示一步完成)关系相互转化的有( )
(“→”表示一步完成)关系相互转化的有( )
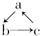 (“→”表示一步完成)关系相互转化的有( )
(“→”表示一步完成)关系相互转化的有( )| 物质 编号 | a | b | c |
| 1 | Na | Na2O2 | NaCl |
| 2 | NaOH | NaHCO3 | Na2CO3 |
| 3 | Al2O3 | NaAlO2 | Al(OH)3 |
| 4 | AlCl3 | Al(OH)3 | NaAlO2 |
| 5 | FeO | Fe(NO3)2 | Fe(OH)2 |
| 6 | MgCl2 | Mg(OH)2 | MgO |
| 7 | CuO | CuSO4 | Cu(OH)2 |
| 8 | Si | SiO2 | H2SiO3 |
| 9 | C | CO | CO2 |
| A. | 1项 | B. | 2项 | C. | 3项 | D. | 4项 |
20.下列说法中不正确的是( )
| A. | 氢氟酸密闭存放于玻璃瓶中 | |
| B. | 硅主要以氧化物和硅酸盐形式存在于自然界中 | |
| C. | 铝是地壳中含量最多的金属元素 | |
| D. | 钢是用量最大、用途最广泛的合金 |
17.分子式为C8H16O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下能转化成C.则有机物A的可能结构有( )
| A. | 1种 | B. | 2种 | C. | 4种 | D. | 8种 |
4.已知某溶液中存在OH-、H+、NH4+、Cl-4种离子经4位同学测定其浓度大小关系如下,其中不可能正确的是( )
| A. | c(Cl-)>c(NH4+)>c(H+)>c(OH-) | B. | c(Cl-)>c(H+)>c(NH4+)>c(OH-) | ||
| C. | c(NH4+)>c(Cl-)>c(OH-)>c(H+) | D. | c(OH-)>c(H+)>c(Cl-)>c(NH4+) |
2.下列有关化学用语表示正确的是( )
| A. | 乙烯的比例模型: | |
| B. | 甲基的电子式: | |
| C. | 乙醇的分子式C2H6O | |
| D. | 中子数为53、质子数为78的碘原子:${\;}_{53}^{131}$I |