题目内容
16.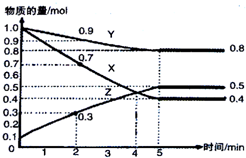 某温度时,在2L容器中X、Y、Z三种气态物质随时间的变化关系曲线如图所示.下列说法正确的是( )
某温度时,在2L容器中X、Y、Z三种气态物质随时间的变化关系曲线如图所示.下列说法正确的是( )| A. | 反应开始到5min,用X表示的反应速率为0.3mol•L-1•min-1 | |
| B. | 反应开始到2min,用Z表示的反应速率为0.05mol•L-1•min-1 | |
| C. | 反应开始到4min反应达到平衡状态 | |
| D. | 反应的化学方程式为:2X(g)+Y(g)?3Z(g) |
分析 A、根据公式v=$\frac{△c}{△t}$来计算;
B、根据公式v=$\frac{△c}{△t}$来计算;
C、化学平衡状态的标志:正逆反应速率相等;
D、根据物质的量的变化判断反应物和生成物,根据物质的量的变化之比等于化学计量数之比书写方程式.
解答 解:A、反应开始到5min,用X表示的反应速率为=$\frac{\frac{1-0.4}{2}}{5}$=0.06mol•(L•min)-1,故A错误;
B、反应开始到2min,用Z表示的反应速率为$\frac{\frac{0.3-0.1}{2}}{2}$=0.05mol•L-1•min-1,故B正确;
C、5min时正逆反应速率相等,化学反应达到了平衡状态,而不是4min,故C错误;
D、由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,且△n(X):△n(Y):△n(Z)=0.6mol:0.2mol:0.4mol=3:1:2,则反应的化学方程式为3X+Y?2Z,故D错误;
故选B.
点评 本题考查化学平衡图象分析题目,题目难度不大,注意分析各物质的量的变化曲线,把握化学方程式的判断方法和化学平衡状态的标志是关键.

练习册系列答案
相关题目
6.一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应:2SO2+O2?2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是( )
| A. | 2 mol SO2+1 mol O2 | B. | 4 mol SO2+1 mol O2 | ||
| C. | 2 mol SO2+1 mol O2+2 SO3 | D. | 3 mol SO2+1 SO3 |
1.氰酸铵(NH4OCN)与尿酸[CO(NH2)2]( )
| A. | 都是共价化合物 | B. | 都是离子化合物 | C. | 互为同素异形体 | D. | 互为同分异构体 |
8.将分别装有500ml0.5mol/L的下列溶液的四个电解池串联在同一电路中,用惰性电极电解,接通直流电源,当电路中有0.2mol的电子通过时,溶液pH值最小的是( )
| A. | KNO3溶液 | B. | AgNO3溶液 | C. | NaCl溶液 | D. | CuCl2溶液 |
5.以下物质间的每步转化同一一步反应不能实现的是( )
| A. | NaHCO3→CO2→Na2CO3 | B. | Fe→FeCl2→FeCl3 | ||
| C. | SiO2→Na2SiO3→H2SiO3 | D. | Al2O3→A1(OH)3→NaAlO2 |
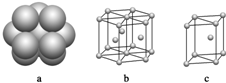 A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素.已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个成单电子,G是ⅠB族的元素.回答下列问题:
A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素.已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个成单电子,G是ⅠB族的元素.回答下列问题: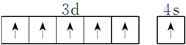 .B、C、D元素的第一电离能由大到小的顺序是N>O>C(用元素符号表示).
.B、C、D元素的第一电离能由大到小的顺序是N>O>C(用元素符号表示).