题目内容
【题目】在固定容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
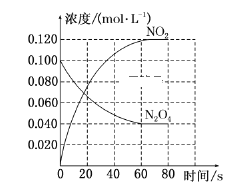
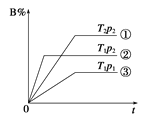
(1)反应的ΔH________(填“大于”或“小于”)0;100 ℃时,体系中各物质浓度随时间变化如上图所示。在0~60 s时段,反应速率v(N2O4)为______________________________。
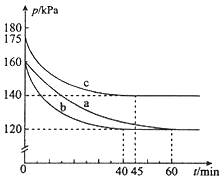
(2)100 ℃时达到平衡后,改变反应温度为T,c(N2O4)降低,经10 s又达到平衡。
①T________(填“大于”或“小于”)100 ℃,判断理由是_____________________;
②100 ℃时达到平衡后,向容器中再充入0.20 mol NO2气体,新平衡建立后,NO2的体积分数________(填“增大”“不变”或“减小”)。
(3)温度T时反应达平衡后,将反应容器的容积减小一半,平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是_____________________________________________。
【答案】大于 0.001 0 mol·L-1·s-1 大于 正反应方向吸热,平衡向吸热方向移动,故温度升高 减小 逆反应 对气体分子数增大的反应,增大压强平衡向逆反应方向移动
【解析】
(1)根据温度对平衡状态的影响分析;根据υ=△c/△t计算;
(2)根据外界条件对平衡状态的影响分析。
(1)根据信息,升高温度,混合气体的颜色变深,说明平衡向正反应方向进行,根据勒夏特列原理,正反应方向为吸热反应,即△H>0;反应速率等于变化浓度和时间的比值,υ(N2O4)=(0.1-0.04)mol/L÷60 s=0.0010 mol/(L·s);
(2)①改变温度,c(N2O4)降低,说明平衡向正反应方向进行。由于正反应是吸热反应,根据勒夏特列原理,应是升高温度,即T>100℃;
②恒容状态下,再充入NO2,相当于在原来的基础上加压,平衡应向体积减小的方向移动,平衡向逆反应方向移动,因此新平衡建立后,NO2的体积分数减小;
(3)容积减少一半,压强增大,根据勒夏特列原理,增大压强,平衡向体积减小方向进行,即向逆反应方向移动。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案【题目】硅铁合金广泛应用于冶金工业,可用于铸铁时的脱氧剂、添加剂等,回答下列问题:
(1)基态Fe原子价层电子的电子排布图为________,基态Si原子电子占据最高能级的电子云轮廓图为________形。
(2)绿帘石的组成为![]() ,将其改写成氧化物的形式为_____________.
,将其改写成氧化物的形式为_____________.
(3)![]() 分子的中心原子的价层电子对数为________,分子的立体构型为________;四卤化硅的熔、沸点如下,分析其变化规律及原因________________________________。
分子的中心原子的价层电子对数为________,分子的立体构型为________;四卤化硅的熔、沸点如下,分析其变化规律及原因________________________________。
|
|
|
| |
熔点/K | 182.8 | 202.7 | 278.5 | 393.6 |
沸点/K | 177.4 | 330.1 | 408 | 460.6 |
(4)![]() 可与乙二胺(
可与乙二胺(![]() ,简写为en)发生如下反应:
,简写为en)发生如下反应:![]()
![]() 。
。![]() 的中心离子的配位数为________;
的中心离子的配位数为________;![]() 中的配位原子为________。
中的配位原子为________。
(5)在硅酸盐中,![]() 四面体(图
四面体(图
|
|
图a | 图b |
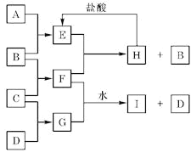
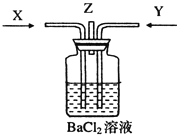
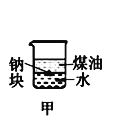
【题目】下列装置所示的实验中,不能达到实验目的是
|
|
|
|
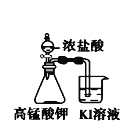
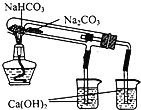
A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)< ρ(钠) < ρ(水) | C.探究氧化性: KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3的热稳定性 |
A. A B. B C. C D. D