题目内容
【题目】A、B、C、D是按原子序数由小到大排列的前20号元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1:2。在一定条件下,各物质之间的相互转化关系如右(部分产物未列出):
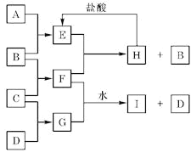
(1)A是_____,C是______ (填元素名称)。
(2)H与盐酸反应生成 E 的化学方程式是_________。
(3)E与F反应的化学方程式是___________。
(4)F与G的水溶液反应生成I和D的离子方程式是_____________。
【答案】碳 钠 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 2CO2+2Na2O2=2Na2CO3+O2 Na2O2+S2-+2H2O=4OH-+S↓+2Na+
【解析】
单质B和C反应生成F,F的焰色反应呈黄色,说明F是钠的化合物,而F是单质B、C化合而成,B、E均为组成空气的成分,故C为金属钠;G是单质C、D化合而成,原子个数比为D:C=1:2,则G中D元素为-2价,且原子序数D>C,故D为硫,G为Na2S;B为单质且为组成空气的成分,还可与钠反应,最易想到是O2,如B为O2,E也为组成空气的成分,由条件分析E只能是CO2,A即为碳,由题中反应关系可知F是Na2O2,据此分析解答。
由分析可知,A、B、C、D分别是:C、O2、Na、S四种单质。
(1)由分析可知,A是碳,C是钠;
(2)A、B是C、O2,反应生成CO2,B、C是O2、Na,反应生成Na2O2,CO2与Na2O2反应生成H和O2,H为Na2CO3,Na2CO3与盐酸反应生成E(二氧化碳)的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)由分析可知E与F分别是CO2与Na2O2,二者反应的化学方程式是2CO2+2Na2O2=2Na2CO3+O2;
(4))F与G分别是Na2O2与Na2S,Na2O2具有强氧化性,将硫从-2价氧化为0价,根据得失电子守恒、电荷守恒,Na2O2与Na2S反应的离子方程式是:Na2O2+S2-+2H2O=4OH-+S↓+2Na+。

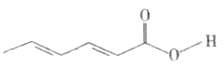
【题目】三氯胺(![]() )是一种饮用水二级消毒剂,可由以下反应制备:Ⅰ.
)是一种饮用水二级消毒剂,可由以下反应制备:Ⅰ.![]()
![]() 。回答下列问题:
。回答下列问题:
(1)已知:Ⅱ.![]()
![]() Ⅲ.
Ⅲ.![]()
![]() ,则
,则![]() ________(用含
________(用含![]() 和
和![]() 的代数式表示)。
的代数式表示)。
(2)向容积均为2 L的甲、乙两个恒温密闭容器中分别加入![]() 和
和![]() ,发生反应Ⅰ,测得两容器中
,发生反应Ⅰ,测得两容器中![]() 随反应时间的变化情况如下表所示:
随反应时间的变化情况如下表所示:
时间/min | 0 | 40 | 80 | 120 | 160 |
容器甲( | 4.0 | 3.0 | 2.2 | 1.6 | 1.6 |
容器乙( | 4.0 | 2.9 | 2.0 | 2.0 | 2.0 |
①0~80 min内,容器甲中![]() ________。
________。
②反应Ⅰ的![]() ________0(填“>”或“<”),其原因为________________________。
________0(填“>”或“<”),其原因为________________________。
③关于反应Ⅰ,下列说法正确的是________(填选项字母)。
a.容器内![]() ,说明反应达到平衡状态
,说明反应达到平衡状态
b.容器内气体密度不变,说明反应达到平衡状态
c.达平衡后,加人一定量![]() ,平衡逆向移动
,平衡逆向移动
d.达平衡后,按原投料比再充入一定量反应物,平衡后![]() 的转化率增大
的转化率增大
④温度为![]() 时HCl(g)的平衡体积分数=________,该温度下,若改为初始体积为2 L的可变容器,平衡时容器中
时HCl(g)的平衡体积分数=________,该温度下,若改为初始体积为2 L的可变容器,平衡时容器中![]() ________(填“>”“=”或“<”)1.6 mol。
________(填“>”“=”或“<”)1.6 mol。
⑤温度为![]() 时,该反应的平衡常数
时,该反应的平衡常数![]() ________。
________。
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
(1)在③~⑦元素中,原子半径最大的是__________(填元素符号);
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________________;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_________。
(4
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________(填物质化学式);呈两性的氢氧化物是_________(填物质化学式),该化合物与NaOH溶液反应的离子方程式为___________。
(6)用电子式表示元素③与⑨形成化合物的过程_____________________________。
【题目】一定温度下,在3个体积均为1.0 L的恒容密闭容器中反应2H2(g)+CO(g)![]() CH3OH(g)达到平衡,下列说法正确的是( )
CH3OH(g)达到平衡,下列说法正确的是( )
容器 | 温度/K | 物质的起始浓度/mol·L-1 | 物质的平衡浓度/mol·L-1 | ||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
Ⅱ | 400 | 0.40 | 0.20 | 0 | |
Ⅲ | 500 | 0.20 | 0.10 | 0 | 0.025 |
A. 该反应的正反应放热
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
【题目】下列实验中,对应的现象以及结论都正确的是
选项 | 实验 | 现象 | 结论 |
A | 碘酒滴到土豆片上 | 土豆片变蓝 | 淀粉遇碘元素变蓝 |
B | 大试管中CH4和Cl2按照1∶1混合,放于光亮处 | 试管内气体颜色变浅,试管壁出现油状液滴,管中有白雾 | 光照条件下,CH4和Cl2发生了化学变化 |
C | 向20%蔗糖溶液中加入少量稀硫酸,加热,再加入新制氢氧化铜后再加热至沸腾 | 无明显现象 | 蔗糖未发生水解 |
D | 小块鸡皮上滴加3~5滴浓硝酸 | 鸡皮由白变黄 | 蛋白质都能发生颜色变化 |
A.AB.BC.CD.D