题目内容
11.汽车排气管加装催化装置,可有效减少CO和NOx的排放.催化装置内发生的反应为:NOx+CO→N2+CO2,下列说法一定正确的是( )| A. | 上述氧化物均为酸性氧化物 | |
| B. | 反应中既有极性键也有非极性键形成 | |
| C. | 当x=2时,转移的电子数为4×6.02×1023 | |
| D. | 该反应为置换反应 |
分析 A、CO为不成盐氧化物;
B、同种非金属元素间形成非极性键,不同非金属元素间形成极性键;
C、x=2时,N元素由NO2中+4价降低为N2中0价,转移电子物质的量为N原子的4倍;
D、反应物中均为化合物.
解答 解:A、CO2为酸性氧化物,CO为不成盐氧化物,故A错误;
B、同种非金属元素间形成非极性键,不同非金属元素间形成极性键,则产物N2中含有非极性键,CO2中含有极性键,故B正确;
C、x=2时,N元素由NO2中+4价降低为N2中0价,转移电子物质的量为N原子的4倍,则生成1molN2,转移电子数为8×6.02×1023,故C错误;
D、一种单质与一种化合物反应生成另一种单质和另一种化合物的反应属于置换反应,所以该反应不是置换反应,故D错误.
故选B.
点评 本题考查化学键、氧化还原反应原理及其计算等,难度中等,注意理解氧化还原反应中电子转移守恒.

练习册系列答案
相关题目
2.下列有关实验的叙述正确的是( )
| A. | 少量液溴、白磷和金属钠的保存均需用水封 | |
| B. | 容量瓶、滴定管在使用前均需用所装试剂润洗 | |
| C. | 苯和甲苯、乙醇和乙酸均可使用分液漏斗分离 | |
| D. | 除去氯化钠固体中的碘、除去碳酸钠固体中的碳酸氢钠,均可用加热的方法 |
19.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 5.4g Al分别与含溶质0.2 mol的NaOH溶液、盐酸反应,生成H2分子数均为0.3NA | |
| B. | 5.35g NH4Cl固体中含有的N-H键个数为0.4NA | |
| C. | 将含有1mol FeCl3的浓溶液全部制成胶体,含Fe(OH)3胶粒的数目为NA | |
| D. | 120g熔融的NaHSO4中含阳离子总数为2NA |
16. 在密闭容器中通入NO和CO各2mol发生反应:2NO(g)+2CO(g)?2CO2(g)+N2(g).容器内CO2随温度(T)、压强(P)和时间(t)的变化曲线如图所示.以下说法合理的是( )
在密闭容器中通入NO和CO各2mol发生反应:2NO(g)+2CO(g)?2CO2(g)+N2(g).容器内CO2随温度(T)、压强(P)和时间(t)的变化曲线如图所示.以下说法合理的是( )
 在密闭容器中通入NO和CO各2mol发生反应:2NO(g)+2CO(g)?2CO2(g)+N2(g).容器内CO2随温度(T)、压强(P)和时间(t)的变化曲线如图所示.以下说法合理的是( )
在密闭容器中通入NO和CO各2mol发生反应:2NO(g)+2CO(g)?2CO2(g)+N2(g).容器内CO2随温度(T)、压强(P)和时间(t)的变化曲线如图所示.以下说法合理的是( )| A. | 温度T2>T1 | B. | 压强P2>P1 | ||
| C. | II曲线表示NO平衡转化率为25% | D. | 该反应的焓变△H<0 |
3.下列关于有机化合物的说法正确的是( )
| A. | 纤维素可以水解生成葡萄糖,因此纤维素属于基本营养物质 | |
| B. | 戊烷(C5H12)有两种同分异构体 | |
| C. | 苯、溴苯、乙醇可以用水鉴别 | |
| D. | 乙醇可以直接氧化成乙酸 |
20.已知碳碳单键可以绕键轴自由旋转,结构简式为如图所示的烃,下列说法中不正确的是( )


| A. | 等质量的该烃和甲烷均完全燃烧,耗氧量前者小于后者 | |
| B. | 该烃能使酸性高锰酸钾溶液褪色,属于苯的同系物 | |
| C. | 分子中一定有11个碳原子处于同一平面上 | |
| D. | 该烃的一氯取代产物为5种 |
1.硫化氢的转化是资源利用和环境保护的重要研究课题.下列关于硫化氢的说法错误的是( )

| A. | H2S是一种弱电解质 | |
| B. | 可用石灰乳吸收H2S气体 | |
| C. | 根据如图可知FeCl3、CuCl2均能氧化H2S | |
| D. | H2S在空气中燃烧可以生成SO2 |
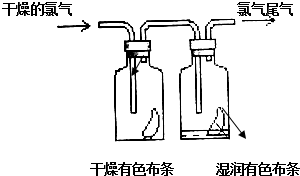 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.

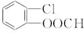

 )常用作香豆素的替代品.鉴别二氢香豆素和它的一种同分异构体(
)常用作香豆素的替代品.鉴别二氢香豆素和它的一种同分异构体( )需要用到的试剂有:NaOH溶液、稀硫酸、氯化铁溶液
)需要用到的试剂有:NaOH溶液、稀硫酸、氯化铁溶液 +CH2═CHCOOCH3$→_{碱}^{Pd}$
+CH2═CHCOOCH3$→_{碱}^{Pd}$ +HBr.
+HBr.