题目内容
6.用下列:①H2O ②H2O2③Ba(OH)2④Na2O2⑤Cl2⑥Ar⑦CO2等物质填空. (1-4小题填序号)(1)由离子键和非极性键构成的是④
(2)由极性键和非极性键构成的是②
(3)不存在化学键的是⑥
(4)共价化合物有①②⑦
(5)写出下列物质的电子式:Na2O2
 .
.
分析 ①H2O中只含O-H共价键;
②H2O2中含O-H极性共价键和O-O非极性共价键;
③Ba(OH)2中含O-H极性共价键和离子键;
④Na2O2中含O-O非极性共价键和离子键;
⑤Cl2中含Cl-Cl非极性共价键;
⑥Ar中不含化学键;
⑦CO2中只含C、O之间极性共价键.
解答 解:①H2O中只含O-H共价键;
②H2O2中含O-H极性共价键和O-O非极性共价键;
③Ba(OH)2中含O-H极性共价键和离子键;
④Na2O2中含O-O非极性共价键和离子键;
⑤Cl2中含Cl-Cl非极性共价键;
⑥Ar中不含化学键;
⑦CO2中只含C、O之间极性共价键,
(1)由离子键和非极性键构成的是④,故答案为:④;
(2)由极性键和非极性键构成的是②,故答案为:②;
(3)不存在化学键的是⑥,故答案为:⑥;
(4)共价化合物有①②⑦,故答案为:①②⑦;
(5)Na2O2的电子式为 ,故答案为:
,故答案为: .
.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
16.下列说法中错误的是( )
| A. | 燃烧、酸碱中和反应都是放热反应 | |
| B. | 化学反应必然伴随着能量的变化 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量 |
17.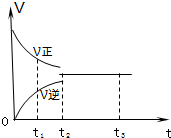 如图是可逆反应3X2+Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应3X2+Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )
 如图是可逆反应3X2+Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应3X2+Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )| A. | t1时,只有正方向反应没有逆方向反应 | |
| B. | t2时,反应已达到平衡状态 | |
| C. | t2-t3,各物质的浓度不再发生变化 | |
| D. | t2-t3,处于静止状态,反应不再发生 |
1.下列各组性质比较中,不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4 | B. | 碱性:KOH>NaOH>LiOH | ||
| C. | 单质的氧化性:F2<Cl2<Br2<I2 | D. | 单质的还原性:Al<Mg<Na |
11.下列实验中,溶液颜色不会发生变化的是( )
| A. | SO2通入品红溶液 | B. | 碘酒滴入淀粉溶液 | ||
| C. | 乙烯通入酸性KMnO4溶液中 | D. | Cl2通入NaOH溶液中 |
18.下列哪种说法可以证明恒温恒容下,可逆反应.N2(g)+3H2(g)?2NH3(g)已达到平衡状态( )
| A. | 混合气体的密度不再改变 | |
| B. | 混合气体的平均分子量不再改变 | |
| C. | 混合气体中,N2、H2、NH3的物质的量之比为1:3:2 | |
| D. | 1个N≡N键断裂的同时,有6个N-H键形成 |
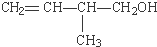 的键线式
的键线式
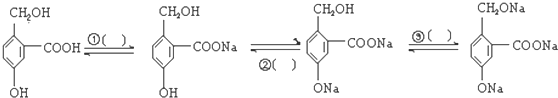
 .
.