题目内容
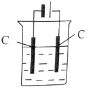
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4)的装置如右图所示。下列说法正确的是

A.铁是阳极,电极反应为Fe-2e-+2OH-![]() Fe(OH)2
Fe(OH)2
B.电解一段时间后,镍电极附近溶液的pH减小
C.若离子交换膜为阴离子交换膜,则电解结束后左侧溶液中含有FeO42-
D.每制得1mol Na2FeO4,理论上可以产生67.2L气体
【答案】C
【解析】
试题分析: A.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸钠(Na2FeO4),铁失电子生成高铁酸钠,则铁作阳极,镍作阴极,电极反应式为Fe+8OH--6e-=FeO42-+4H2O,A错误;B.镍电极上氢离子放电生成氢气,氢离子浓度减小,所以溶液的pH增大,B错误;C.若离子交换膜为阴离子交换膜,则电解结束后由于浓度差左侧溶液中会含有FeO42-,C正确;D.温度和压强未知,所以无法计算生成气体体积,D错误;答案选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目