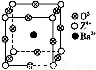
题目内容
绿原酸是一种新型高效的酚型天然抗氧化剂,在食品行业有着广泛的用途,在某些食品中可取代或部分取代目前常用的人工合成的抗氧化剂。
绿原酸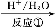
 +
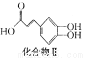
+
(1)在反应①中,绿原酸与水按1∶1发生反应,则绿原酸的分子式为 ,反应①反应类型为 。
(2)1 mol化合物Ⅰ与足量金属钠反应生成标准状况下氢气体积为 。
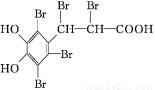
(3)写出化合物Ⅱ与浓溴水反应的化学反应方程式: 。
(4)1 mol化合物Ⅱ与足量的试剂X反应得到化合物Ⅲ( ),则试剂X是 。
),则试剂X是 。
(5)化合物Ⅳ有如下特点:①与化合物Ⅱ互为同分异构体;②遇FeCl3溶液显色;③1 mol化合物Ⅳ与足量银氨溶液反应生成4 mol Ag;④苯环上的一卤代物只有一种。写出化合物Ⅳ的一种可能的结构简式: 。
(1)C16H18O9 取代反应
(2)56 L
(3)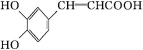 +4Br2
+4Br2
 +3HBr
+3HBr
(4)NaHCO3溶液
(5)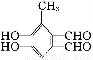 (或
(或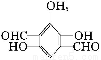 或
或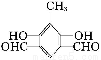 )
)
【解析】(1)根据绿原酸与水按1∶1发生反应生成化合物Ⅰ和Ⅱ,化合物Ⅰ和Ⅱ的分子式分别为C7H12O6、C9H8O4,将化合物Ⅰ和Ⅱ的分子式相加再减去1个水分子,即得绿原酸的分子式为C16H18O9;根据反应条件和过程可判断发生的是取代反应。
(2)1 mol化合物Ⅰ含有4 mol—OH和1 mol—COOH与足量金属钠反应,故1 mol化合物Ⅰ能与5 mol金属钠反应,生成2.5 mol H2,即标况下56 L。
(3)化合物Ⅱ中含有碳碳双键和酚羟基官能团,而酚羟基的邻对位能与溴水发生取代反应,故1mol化合物Ⅱ能与4mol溴水反应,故方程式为 +4Br2
+4Br2
 +3HBr。
+3HBr。
(4)试剂X能与—COOH反应而不能与—OH反应,则试剂X为NaHCO3溶液。
(5)Ⅳ遇FeCl3溶液显色则一定含有苯环和酚羟基,1 mol化合物Ⅳ与足量银氨溶液反应生成4 mol Ag,则说明含有2个—CHO,苯环上的一卤代物只有一种,则化合物Ⅳ可以为 、
、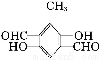 或
或 等,任写其中一种即可。
等,任写其中一种即可。

阿司匹林(乙酰水杨酸,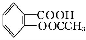 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135 ℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
乙酸酐+水杨酸
 粗产品
粗产品
 乙酰水杨酸
乙酰水杨酸
(阿司匹林) 测熔点
测熔点
主要试剂和产品的物理常数
名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
水杨酸 | 138 | 158(熔点) | 微溶 |
醋酸酐 | 102 | 139.4(沸点) | 反应 |
乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是 。
(2)①合成阿司匹林时,最合适的加热方法是 。
②加热后冷却,未发现被冷却容器中有晶体析出,此时应采取的措施是 。
③抽滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是 。
(3)试剂A是 。
另一种改进的提纯方法如下:
粗产品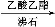
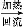
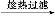
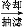
 乙酰水杨酸
乙酰水杨酸
(4)改进的提纯方法中加热回流的装置如图所示,
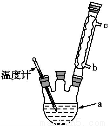
①使用温度计的目的是 。
②此种提纯方法中乙酸乙酯的作用是: ,所得产品的有机杂质要比原方案少,原因是 。