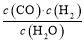题目内容
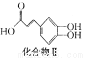
已知X、Y和Z三种元素的原子序数之和等于48。X是有机物主要组成元素。X的一种1∶1型气态氢化物分子中既有σ键又有π键。Z是金属元素,Z的核电荷数小于28,且次外层有2个未成对电子。
(1)X在该氢化物中以 方式杂化。X和Y形成的化合物的熔点应该 (填“高于”或“低于”)X氢化物的熔点。
(2)Y在周期表中位于 ;Z4+的核外电子排布式为 。
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看作一种含氧酸盐)。经X射线分析,M晶体的最小重复单位为正方体(如图),边长为4.03×10-10 m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
①制备M的化学反应方程式是 (Z用元素符号表示)。
②在M晶体中,Ba2+的氧配位数(Ba2+周围等距且最近的O2-的数目)为 。
③晶体M密度的计算式为ρ= (Z相对原子质量为48)。
(1)sp 高于 (2)第4周期ⅡA族 1s22s22p63s23p6
(3)①TiO2+BaCO3 BaTiO3+CO2↑ ②12
BaTiO3+CO2↑ ②12
③(137+48+3×16)/NA(4.03×10-8)3 g·cm-3
【解析】有机物的主要组成元素X为碳元素,Z元素次外层有2个未成对电子且核电荷数小于28,只能为过渡元素钛22Ti,位于周期表中第4周期ⅣB族。根据原子序数之和为48,可推知Y为20号元素钙。(1)X的该氢化物为乙炔,乙炔为直线形分子,碳原子以sp方式杂化,碳化钙是离子化合物,熔点高于碳的氢化物分子晶体熔点。(2)钙元素在周期表中第4周期ⅡA族。钛离子核外电子排布式为:1s22s22p63s23p6。(3)①用均摊法可以推出M的化学式为BaTiO3,制备BaTiO3化学方程式:TiO2+BaCO3 BaTiO3+CO2↑。②与钡离子紧邻等距的氧离子共有12个。③由1 mol该化合物的体积关系得:
BaTiO3+CO2↑。②与钡离子紧邻等距的氧离子共有12个。③由1 mol该化合物的体积关系得: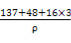 =(4.03×10-8)3NA,整理得ρ=
=(4.03×10-8)3NA,整理得ρ=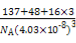 g·cm-3。
g·cm-3。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案下列实验或操作不能达到目的的是( )
A.用溴水鉴别乙醇、苯和四氯化碳
B.用稀硫酸和银氨溶液可以检验淀粉已部分水解
C.用饱和碳酸钠溶液除去乙酸乙酯中的少量乙酸
D.用饱和碳酸钠溶液鉴别乙酸乙酯、乙醇和乙酸
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)已知在25 ℃、101 kPa时,C(s)、H2(g)和CO(g)燃烧的热化学方程式分别为:
C(s)+O2(g)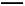 CO2(g) ΔH1=-393.5 kJ/mol;
CO2(g) ΔH1=-393.5 kJ/mol;
H2(g)+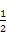 O2(g)
O2(g)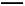 H2O(g) ΔH2=-241.8 kJ/mol;
H2O(g) ΔH2=-241.8 kJ/mol;
CO(g)+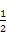 O2(g)
O2(g)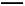 CO2(g) ΔH3=-283.0 kJ/mol;
CO2(g) ΔH3=-283.0 kJ/mol;
①则C(s)+H2O(g) CO(g)+H2(g) ΔH= ,该反应平衡常数的表达式为K= ;升高温度,则K值 (填“变大”、“变小”或“不变”)。
CO(g)+H2(g) ΔH= ,该反应平衡常数的表达式为K= ;升高温度,则K值 (填“变大”、“变小”或“不变”)。
②如果①反应在容积不变的密闭容器中进行,当反应达到平衡时 (填编号)。
a.v正(CO)∶v逆(H2)=1∶1
b.碳的质量保持不变
c.v正(CO)=v逆(H2O)
d.容器中的压强不变
③在容积不变的密闭容器中进行①反应,可以使c(CO)增大的是 。
a.升高温度
b.充入He(g),使体系压强增大
c.将H2(g)从体系中分离出来
d.加入催化剂
(2)将不同量的CO(g)和H2O(g)分别通入体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下2组数据:
CO2(g)+H2(g),得到如下2组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
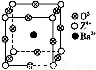
①实验1中以v(CO2)表示的反应速率为 。
②向实验2的平衡混合物中再加入0.4 mol H2O(g)和0.4 mol CO2,达到新平衡时CO的转化率 (填“变大”、“变小”或“不变”)。