题目内容
【题目】某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2的实验,其流程如下:
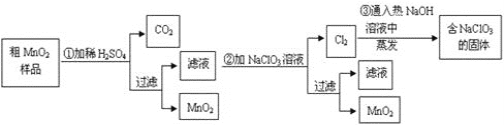
(1)第①步加稀H2SO4时,粗MnO2样品中的____(写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式:_________
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、酒精灯 、______、______,已知蒸发得到的固体中有NaClO3和NaOH,则一定还有____(写物质名称)。
(4)若粗MnO2样品的质量为12.69 g,第①步反应后,过滤得到8.7 gMnO2,并收集到0.224 L CO2(标准状况),则第②步反应中至少需要_______ g NaClO3。
【答案】MnO 、MnCO3 5Mn2++2ClO3-+4H2O=5MnO2↓+Cl2↑+8H+ 蒸发皿 玻璃棒 氯化钠 2.13
【解析】
(1)从流程看,第①步加稀H2SO4时,粗MnO2样品中只有MnO2不溶解,另两种物质都被硫酸溶解,转化为可溶性物质。
(2)第②步反应,是滤液中的Mn2+被ClO3-氧化为MnO2,ClO3-被还原为Cl2。
(3)第③步蒸发操作,应在蒸发皿中进行,使用玻璃棒搅拌,从而得出缺少的仪器,已知蒸发得到的固体中有NaClO3和NaOH,则一定还有Cl2的还原产物。
(4)若粗MnO2样品的质量为12.69 g,第①步反应后,过滤得到8.7 gMnO2,并收集到0.224 L CO2(标准状况),则MnCO3的物质的量为![]() =0.01mol,质量为0.01mol×115g/mol=1.15g,MnO的质量为12.69g-8.7 g-1.15g=2.84g,物质的量为
=0.01mol,质量为0.01mol×115g/mol=1.15g,MnO的质量为12.69g-8.7 g-1.15g=2.84g,物质的量为![]() ,则n(Mn2+)=0.01mol+0.04mol=0.05mol,依据第②步反应的离子方程式,可求出需要NaClO3的质量。
,则n(Mn2+)=0.01mol+0.04mol=0.05mol,依据第②步反应的离子方程式,可求出需要NaClO3的质量。
(1)从流程看,第①步加稀H2SO4时,粗MnO2样品中只有MnO2不溶解,MnO、MnCO3都被硫酸溶解,转化为可溶性物质。答案为:MnO、MnCO3;
(2)第②步反应,是滤液中的Mn2+被ClO3-氧化为MnO2,ClO3-被还原为Cl2,反应的离子方程式为5Mn2++2ClO3-+4H2O=5MnO2↓+Cl2↑+8H+。答案为:5Mn2++2ClO3-+4H2O
=5MnO2↓+Cl2↑+8H+;
(3)第③步蒸发操作,应在蒸发皿中进行,使用玻璃棒搅拌,从而得出缺少的仪器为蒸发皿、玻璃棒;已知蒸发得到的固体中有NaClO3和NaOH,则一定还有Cl2的还原产物氯化钠。答案为:蒸发皿;玻璃棒;氯化钠;
(4)若粗MnO2样品的质量为12.69 g,第①步反应后,过滤得到8.7 gMnO2,并收集到0.224 L CO2(标准状况),则MnCO3的物质的量为![]() =0.01mol,质量为0.01mol×115g/mol=1.15g,MnO的质量为12.69g-8.7 g-1.15g=2.84g,物质的量为
=0.01mol,质量为0.01mol×115g/mol=1.15g,MnO的质量为12.69g-8.7 g-1.15g=2.84g,物质的量为![]() ,则n(Mn2+)=0.01mol+0.04mol=0.05mol,依据第②步反应的离子方程式5Mn2++2ClO3-+4H2O=5MnO2↓+Cl2↑+8H+,可求出需要NaClO3的物质的量为0.02mol,质量为0.02mol×106.5g/mol=2.13g。答案为:2.13。
,则n(Mn2+)=0.01mol+0.04mol=0.05mol,依据第②步反应的离子方程式5Mn2++2ClO3-+4H2O=5MnO2↓+Cl2↑+8H+,可求出需要NaClO3的物质的量为0.02mol,质量为0.02mol×106.5g/mol=2.13g。答案为:2.13。

【题目】下列实验过程可以达到实验目的的是
编号 | 实验目的 | 实验过程 |
A | 配制0.4000 mol·L1的NaOH溶液 | 称取4.0 g固体NaOH于烧杯中,加入250 mL蒸馏水溶解,然后转移至250 mL容量瓶中定容 |
B | 探究维生素C的还原性 | 向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
C | SO42-的检验 | 先滴加BaCl2溶液再滴加HCl溶液生成白色沉淀证明原溶液中有SO42- |
D | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色。 | 溶液中一定含有Fe2+ |
A.AB.BC.CD.D