题目内容
在某密闭容器中,可逆反应:A(g)+B(g)?xC(g),符合下列图象(Ⅰ)所示关系.由此推断对图象(Ⅱ)的正确说法是( )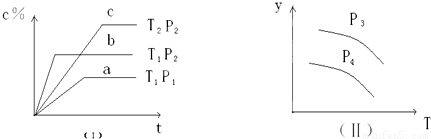
A.P3>P4,y轴表示A的百分含量
B.P3<P4,y轴表示B的百分含量
C.P3<P4,y轴表示混合气体的密度
D.P3>P4,y轴表示混合气体的平均相对分子质量
【答案】分析:由图(1)可知,压强为P2时,温度T1先到达平衡,故温度T1>T2,且温度越高,平衡时C的质量分数越低,故升高温度平衡向逆反应移动,正反应为放热反应;
温度为T1时,压强P2先到达平衡,故压强P2>P1,且压强越大,平衡时C的质量分数越高,故增大压强平衡向正反应移动,正反应为体积减小的反应,故x=1,
由图(2)可知,升高温度,平衡向逆反应方向移动,y值减小,则y可为A、B的百分含量、C的体积分数等,结合压强对平衡移动的影响分析.
解答:解:由图(1)可知,压强为P2时,温度T1先到达平衡,故温度T1>T2,且温度越高,平衡时C的质量分数越低,故升高温度平衡向逆反应移动,正反应为放热反应;
温度为T1时,压强P2先到达平衡,故压强P2>P1,且压强越大,平衡时C的质量分数越高,故增大压强平衡向正反应移动,正反应为体积减小的反应,故x=1,则:
A.如果P3>P4,在相同温度下增大压强平衡向正反应方向移动,则A的A的百分含量减小,同时升高温度平衡向逆反应方向移动,A的百分含量增大,图象与实际不符,故A错误;
B.P3<P4,增大压强,平衡向正反应移动,B的含量减小,同时升高温度平衡向逆反应方向移动,B的含量应增大,图象与实际不符,故B错误;
C.混合气体的总质量不变,容器的体积不变,混合气体的密度不变,故C错误;
D.P3>P4,增大压强,平衡向正反应移动,混合气体总的物质的量减小,混合气体的总质量不变,平均相对分子质量增大,温度升高平衡向逆反应移动,混合气体总的物质的量增大,平均相对分子质量减小,图象与实际相符,故D正确;
故选D.
点评:本题考查化学平衡图象、化学平衡的影响因素等,难度中等,注意根据图(1)分析反应的特征是解题的关键.
温度为T1时,压强P2先到达平衡,故压强P2>P1,且压强越大,平衡时C的质量分数越高,故增大压强平衡向正反应移动,正反应为体积减小的反应,故x=1,
由图(2)可知,升高温度,平衡向逆反应方向移动,y值减小,则y可为A、B的百分含量、C的体积分数等,结合压强对平衡移动的影响分析.
解答:解:由图(1)可知,压强为P2时,温度T1先到达平衡,故温度T1>T2,且温度越高,平衡时C的质量分数越低,故升高温度平衡向逆反应移动,正反应为放热反应;
温度为T1时,压强P2先到达平衡,故压强P2>P1,且压强越大,平衡时C的质量分数越高,故增大压强平衡向正反应移动,正反应为体积减小的反应,故x=1,则:
A.如果P3>P4,在相同温度下增大压强平衡向正反应方向移动,则A的A的百分含量减小,同时升高温度平衡向逆反应方向移动,A的百分含量增大,图象与实际不符,故A错误;
B.P3<P4,增大压强,平衡向正反应移动,B的含量减小,同时升高温度平衡向逆反应方向移动,B的含量应增大,图象与实际不符,故B错误;
C.混合气体的总质量不变,容器的体积不变,混合气体的密度不变,故C错误;
D.P3>P4,增大压强,平衡向正反应移动,混合气体总的物质的量减小,混合气体的总质量不变,平均相对分子质量增大,温度升高平衡向逆反应移动,混合气体总的物质的量增大,平均相对分子质量减小,图象与实际相符,故D正确;
故选D.
点评:本题考查化学平衡图象、化学平衡的影响因素等,难度中等,注意根据图(1)分析反应的特征是解题的关键.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目