题目内容
10.在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明反应:A(s)+3B(g)═2C(g)+D(g) 已达平衡状态的是( )| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | 3v逆(C)=2v正(B) | D. | 气体的平均相对分子质量 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、反应前后两边气体计量数相等,所以体系的压强始终不变,所以不能说明反应达平衡状态,故A选;
B、混合气体的密度,容器内气体的质量不变,说明反应达平衡状态,故B不选;
C、3v逆(C)=2v逆(B)=2v正(B),所以正逆反应速率相等,反应达平衡状态,故C不选;
D、反应前后两边气体计量数相等,气体的平均相对分子质量不变,则容器内气体的质量不变,说明反应达平衡状态,故D不选;
故选A.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
15.下列说法中正确的是( )
| A. | 金刚石晶体中的最小碳原子环由6个碳原子构成 | |
| B. | 金刚石晶体中的碳原子是sp2杂化的 | |
| C. | 12g金刚石中含有C-C键的个数为4NA | |
| D. | 金刚石化学性质稳定,即使在高温下也不会和O2反应 |
5.金属钛(Ti)硬度大、熔点高、常温下耐酸碱腐蚀,被誉为“未来金属”.以钛铁矿[主要成分FeTiO3,含FeO、Al2O3、SiO2等杂质]为主要原料冶炼金属钛并获得副产品绿矾(FeSO4•7H2O)的工业生产流程如图1:
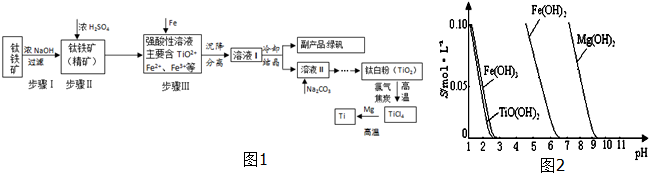
(1)钛铁矿精矿和浓硫酸反应的产物之一是TiOSO4,反应中无气体生成.试写出反应化学方程式:FeTiO3+H2SO4(浓)=TiOSO4+FeSO4+2H2O;
(2)已知:TiO2+易水解,只能存在于强酸性溶液中. 25℃时,难溶电解质溶解度(s)与pH关系如图2,TiO(OH)2溶度积Ksp=1×10-29,若溶液中残留c(TiO2+)=1.0×10-5 mol•L-1,则调节溶液pH至少为3;步骤Ⅲ加入铁屑原因是将Fe3+转化为Fe2+,防止Fe3+与TiO2+同时生成沉淀.
(3)对溶液Ⅱ进行加热,同时加入Na2CO3粉末的作用加热促进TiO2++2H2O?TiO(OH)2+2H+ 右移,Na2CO3粉末消耗H+,促进TiO2+水解;
(4)钛白粉与氯气、焦炭在高温下进行反应,还生成一种可燃性无色气体,写出该反应的化学方程式
TiO2+2Cl2+2C 高温_ TiCl4+2CO,该生产流程工艺中,可以循环使用的物质为H2SO4(填化学式)
(5)Mg还原TiCl4反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于1412℃即可.
(6)为了测定绿矾中所含结晶水个数,可取样品进行灼烧,在灼烧时需要仪器除了三脚架、坩埚、石棉网、坩埚钳、酒精喷灯外还需要泥三角、玻璃棒.(填仪器名称)

(1)钛铁矿精矿和浓硫酸反应的产物之一是TiOSO4,反应中无气体生成.试写出反应化学方程式:FeTiO3+H2SO4(浓)=TiOSO4+FeSO4+2H2O;
(2)已知:TiO2+易水解,只能存在于强酸性溶液中. 25℃时,难溶电解质溶解度(s)与pH关系如图2,TiO(OH)2溶度积Ksp=1×10-29,若溶液中残留c(TiO2+)=1.0×10-5 mol•L-1,则调节溶液pH至少为3;步骤Ⅲ加入铁屑原因是将Fe3+转化为Fe2+,防止Fe3+与TiO2+同时生成沉淀.
(3)对溶液Ⅱ进行加热,同时加入Na2CO3粉末的作用加热促进TiO2++2H2O?TiO(OH)2+2H+ 右移,Na2CO3粉末消耗H+,促进TiO2+水解;
(4)钛白粉与氯气、焦炭在高温下进行反应,还生成一种可燃性无色气体,写出该反应的化学方程式
TiO2+2Cl2+2C 高温_ TiCl4+2CO,该生产流程工艺中,可以循环使用的物质为H2SO4(填化学式)
(5)Mg还原TiCl4反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于1412℃即可.
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/℃ | 136.4 | 1090 | 1412 | 3287 |
2.工业生产苯乙烯是利用乙苯的脱氢反应: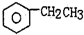 (g)560℃?
(g)560℃?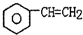 (g)+H2(g)△H<0
(g)+H2(g)△H<0
针对上述反应,在其它条件不变时,下列说法正确的是( )
 (g)560℃?
(g)560℃?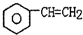 (g)+H2(g)△H<0
(g)+H2(g)△H<0针对上述反应,在其它条件不变时,下列说法正确的是( )
| A. | 加入适当催化剂,可以提高乙苯的转化率 | |
| B. | 在保持体积一定的条件下,充入较多的乙苯,可以提高乙本的转化率 | |
| C. | 在加入乙苯至达到平衡过程中,混合气体的平均相对分子质量不变 | |
| D. | 仅从平衡移动的角度分析,工业生产苯乙稀选择恒压条件优于恒容条件 |
19.氯气可用消灭田鼠,为此将氯气通过软管灌入洞中,这是利用了氯气下列性质中的( )
①黄绿色 ②密度比空气大 ③有毒 ④较易液化 ⑤溶解于水.
①黄绿色 ②密度比空气大 ③有毒 ④较易液化 ⑤溶解于水.
| A. | ②③ | B. | ③④ | C. | ①②③ | D. | ③④⑤ |
20.下列反应不属于氧化还原反应的是( )
| A. | CuSO4+2NaOH═Cu(OH)2↓+Na2SO4 | B. | Cl2+H2O?HCl+HClO | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | 2Cu+O2△_2CuO |
 乙烯气相直接水合反应,在其他条件相同时,分别测得C2H4的平衡转化率在不同压强(P1、P2)下随温度变化的曲线如图.结合曲线归纳平衡转化率
乙烯气相直接水合反应,在其他条件相同时,分别测得C2H4的平衡转化率在不同压强(P1、P2)下随温度变化的曲线如图.结合曲线归纳平衡转化率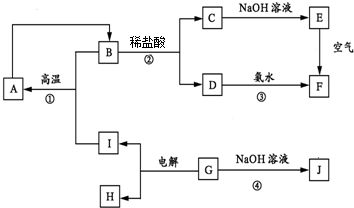
 ,E的化学式为Fe(OH)2.
,E的化学式为Fe(OH)2.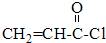
 .(注明反应条件)
.(注明反应条件) 或CH2=CH-O-CH2-O-CH=CH2.
或CH2=CH-O-CH2-O-CH=CH2.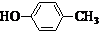 也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为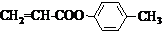 .
.