题目内容
13. 乙烯是重要的石油化工产品.回答下列问题.
乙烯是重要的石油化工产品.回答下列问题.(1)下列物质中,通过乙烯加成反应,无法得到的是B(填序号)
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
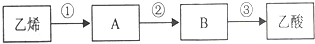
(2)已知2CH3CHO+O2$→_{加热}^{催化剂}$2CH3COOH.若以乙烯为主要原料合成乙酸,其合成线路如图所示.反应②的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(3)工业上以乙烯为原料可以生产一种重要的合成高分子化合物,其反应的化学方程式为
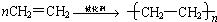 ,反应类型是加聚反应.
,反应类型是加聚反应.
分析 乙烯含有碳碳双键,可发生加成、加聚和氧化反应,由转化关系可知A为乙醇,B为乙醛,乙醛氧化生成乙酸,以此解答该题.
解答 解:(1)乙烯和溴化氢发生加成生成溴乙烷,和水加成生成乙醇,和氢气加成生成乙烷,不能生成CH3CHCl2,故答案为:B;
(2)乙醇催化氧化生成乙醛,反应的化学方程式为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O;
(3)乙烯发生加成聚合反应生成聚乙烯,反应的方程式为: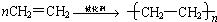 ;
;
故答案为: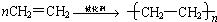 ;加聚反应.
;加聚反应.
点评 本题主要考查有机物的推断,为高频考点,题目侧重于学生乙烯的化学性质,注重了基础知识的考查,难度不大.

练习册系列答案
相关题目
3.下列各有机物中,在常温常压下为无色液体,且比水重的是( )
①苯 ②硝基苯 ③溴苯 ④四氯化碳.
①苯 ②硝基苯 ③溴苯 ④四氯化碳.
| A. | ①③④ | B. | ②③④ | C. | ①② | D. | 全部 |
4.下列有关电化学的叙述正确的是( )
| A. | 在原电池的负极和电解池的阴极上都发生氧化反应 | |
| B. | 镀层被破坏后,镀锡铁板比镀锌铁板更耐腐蚀 | |
| C. | 氢氧燃料电池的负极上发生的电极反应式为:O2+2H2O+4e-═4OH- | |
| D. | 用惰性电极电解饱和食盐水时,若转移电子数为6.02×1023,则生成NaOH的物质的量为1mol |
1.下列对化学反应的认识,错误的是( )
| A. | 会引起化学键的变化 | B. | 会产生新物质 | ||
| C. | 物质间必然发生电子转移 | D. | 必然伴随着能量的变化 |
8.已知:合成氨反应(即N2+3H2═2NH3)为放热反应.反应过程中断裂1molN≡N消耗的能量为Q1kJ,断裂1molH-H消耗的能量为Q2kJ,断裂1molN-H消耗的能量为Q3kJ.下列关系式中正确的是( )
| A. | Q1+3Q2<6Q3 | B. | Q1+3Q2>2Q3 | C. | 3Q1+Q2>6Q3 | D. | Q1+3Q2<2Q3 |
18.下列有关物质的性质或应用的说法正确的是( )
| A. | 石油裂化的主要产品是甲烷、乙烯和苯 | |
| B. | 脂肪属于高分子化合物 | |
| C. | 盐析可提纯蛋白质并能保持蛋白质的生理活性 | |
| D. | 木糖醇(C5H12O5)是一种甜味剂,与葡萄糖互为同系物 |
2.已知:4A(g)+5B(g)═4C(g)+6D(g),如果反应速率分别用V(A)、V(B)、V(C)、V(D)表示,正确的关系是( )
| A. | $\frac{4}{5}$ V(A)=V(B) | B. | $\frac{5}{6}$V(B)=V(D) | C. | $\frac{2}{3}$ V(A)=V(D) | D. | $\frac{4}{5}$ V(B)=V(C) |
3.下列第三周期元素中,非金属性最弱的是( )
| A. | 硅 | B. | 氯 | C. | 磷 | D. | 硫 |
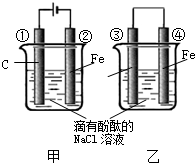 化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.
化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.