题目内容
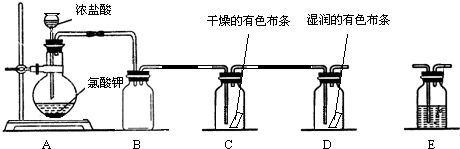
14.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).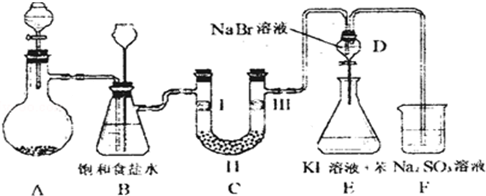
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入d.
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是E中溶液分为两层,上层(苯层)为紫红色.
(6)有人提出,装置F中可改用足量的NaHSO3溶液吸收余氯,试写出相应的离子反应方程式:SO32-+Cl2+H2O=SO42-+2Cl-+2H+,判断改用NaHSO3溶液是否可行否(填“是”或“否”).
分析 (1)次氯酸钙与浓盐酸反应生成氯化钙、氯气与水;
(2)盐酸易挥发,反应制取的氯气中含有氯化氢,装置B中饱和食盐水的作用是除去Cl2中的HCl;
装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,发生堵塞时B中的,压强增大;
(3)验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性;
(4)当向D中缓缓通入少量氯气时,氯气和溴化钠反应生成溴单质,溶液显示黄色;
(5)打开活塞,将装置D中少量溶液加入装置E中,生成的溴单质和碘化钾反应生成碘单质,碘单质溶解于苯中,振荡分层,苯层在上层;
(6)氯气具有强氧化性,在溶液中将SO32-氧化SO42-同时生成Cl-、H+.若改用NaHSO3,会发生反应4HSO3-+Cl2=SO42-+2Cl-+3SO2↑+2H2O,生成二氧化硫气体.
解答 解:(1)次氯酸钙与浓盐酸反应生成氯化钙、氯气与水,反应方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,
故答案为:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
(2)盐酸易挥发,反应制取的氯气中含有氯化氢,装置B中饱和食盐水的作用是除去Cl2中的HCl;
装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,发生堵塞时B中的,压强增大,B中长颈漏斗中液面上升,形成水柱,
故答案为:除去Cl2中的HCl;B中长颈漏斗中液面上升,形成水柱;
(3)装置C的实验目的是验证氯气是否具有漂白性,验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性,选项中abc的Ⅱ中都是干燥剂,再通入湿润的有色布条不能验证氯气的漂白性,所以C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,所以选d,故答案为:d;
(4)当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为黄色,说明氯气和溴化钠反应生成溴单质,故答案是:黄;
(5)打开活塞,将装置D中含溴单质的少量溶液加入焓碘化钾和苯的装置E中,溴单质和碘化钾反应生成碘单质,碘单质溶于苯呈紫红色,振荡.观察到的现象是:E中溶液分为两层,上层(苯层)为紫红色,故答案为:E中溶液分为两层,上层(苯层)为紫红色;
(6)氯气具有强氧化性,在溶液中将SO32-氧化SO42-同时生成Cl-、H+,反应离子方程式为SO32-+Cl2+H2O=SO42-+2Cl-+2H+;若改用NaHSO3,会发生反应4HSO3-+Cl2=SO42-+2Cl-+3SO2↑+2H2O,生成二氧化硫气体,二氧化硫污染环境,故不可行.故答案为:SO32-+Cl2+H2O=SO42-+2Cl-+2H+;否.
点评 本题考查了氯气实验室制取、氯气化学性质、实验设计、实验装置的理解评价、化学方程式的书写等,是对所学知识的综合运用,注意基础知识的掌握,本题难度中等.

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案| A. | v(D)=0.5mol•L-1.s-1 | B. | v(C)=3.0 mol•L-1•min-1 | ||
| C. | v(B)=0.30 mol•L-1.s-1 | D. | v(A)=0.60 mol•L-1.s-1 |
| A. | 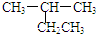 2-乙基丙烷 | B. | 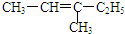 3-甲基-3-戊烯 | C. | 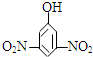 2,4-二硝基苯酚 | D. |  2,3-丁二醇 |
(1)电解氯化钠饱和溶液可以制得多种化工原料,写出电解氯化钠溶液的化学方程式:2NaCl+2H2O $\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.用其中两种原料可以制备常见的消毒剂,
请写出制备反应的离子反应方程式Cl2+2OH-=Cl-+ClO-+H2O.
(2)①若MgCl2粗产品中含有Mg2+、Fe2+、Fe3+、Mn2+ 等阳离子,需先将 Fe2+、Fe3+、Mn2+ 转化为沉淀除去,Fe(OH)2为絮状,常将Fe2+转化为Fe(OH)3除去,若只加入(1)中制备消毒剂时的产物之一,则所加物质的化学式为NaClO,控制溶液的pH为9.8. 请写出该物质与溶液中Fe2+ 反应的离子方程式:2Fe2++ClO-+4OH-+H2O=2Fe(OH)3↓+Cl-.
| 物质 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | Mg(OH)2 |
| 开始沉淀 | 7.6 | 2.7 | 8.3 | 9.9 |
| 沉淀完全 | 9.6 | 3.7 | 9.8 | 11.1 |
(3)如图2为某同学设计的从海带中提取碘单质的流程图.
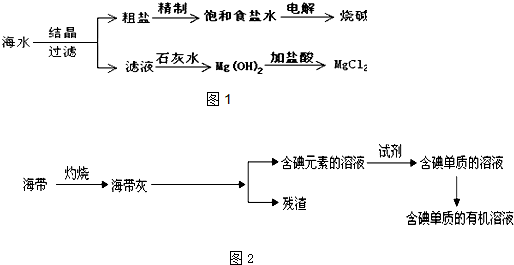
①请写出从海带灰提取碘元素时用到的主要仪器的名称铁架台、烧杯、玻璃棒、漏斗;
②将溶液中的碘元素的转化为碘单质可以用H2O2稀H2SO4试剂,请写出发生反应的离子方程式H2O2+2I-+2H+=I2+2H2O,
含碘单质CCl4溶液呈现紫红色.
| A. | 1,4-二甲基丁烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 2-乙基戊烷 | D. | 4-甲基-3-乙基辛烷 |
| A. | O2与O3 | B. | CH3CH2OH与CH3CH2-O-CH2CH3 | ||
| C. | ${\;}_{6}^{12}$C与${\;}_{6}^{13}$C | D. | CH3CH2CH2CH3与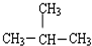 |
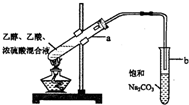
| A. | 向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加入乙酸 | |
| B. | 饱和碳酸钠溶液可以除去乙酸乙酯中混有的乙酸 | |
| C. | 向a试管中加入几块碎瓷片的作用是防止加热时液体暴沸 | |
| D. | 将制得的乙酸乙酯分离出来,应采用“分液”的实验操作 |