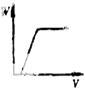��Ŀ����
����Ŀ������������������Һ���й���������ȷ���ǣ�������
�� | �� | �� | �� | |
Ũ��c/mol/L | 0.1 | 0.1 | 0.1 | 0.1 |
��Һ | ��ˮ | CH3COONa��Һ | ���� | ���� |
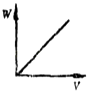
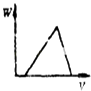
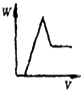
A.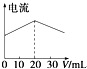 ��20 mL ����Һ����μ������Һ����Һ���������仯��ͼ
��20 mL ����Һ����μ������Һ����Һ���������仯��ͼ
B.�ڡ�������Һ�������ϣ�����Ũ�ȣ�2c��Na+��=c��CH3COO����+c��CH3COOH��
C.�١�������Һ�������ϣ�����Ũ�ȣ�c��Cl������c��NH4+����c��H+����c��OH����
D.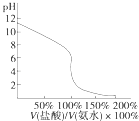 �âܵζ��٣��ζ�������ͼ�����÷�̪��ָʾ��
�âܵζ��٣��ζ�������ͼ�����÷�̪��ָʾ��
���𰸡�D
���������⣺A��һˮ�ϰ��ʹ�����������ʣ�����Ⱥ�С���䷴Ӧ���ɵĴ������ǿ����ʣ��ܹ���ȫ���룬�����ƶ�������Ũ�ȴ���Һ��������ǿ���������Ϻ��ٵ�����ᣬ����Ũ�ȼ�С������������������A��ȷ��
B���������غ㣬�ڡ�������Һ�������ϣ�����Ũ�ȣ�2c��Na+��=c��CH3COO����+c��CH3COOH������B��ȷ��
C���١�������Һ�������������Ȼ����Һ���Ȼ����Һ��笠�����ˮ��ʹ��Һ�����ԣ�����������Ũ��c��Cl������c��NH4+����c��H+����c��OH��������C��ȷ��
D��ǿ������������к͵ζ�ʱ�ü�����ָʾ������D����
��ѡD��
�����㾫����������Ҫ���������������ˮ��Һ�еĵ���ƽ������֪ʶ�㣬��Ҫ���յ�������ʷ����������ӵ����ʵ��ڽ�ϳɷ��ӵ�����ʱ��������ʵĵ���ʹ��ڵ���ƽ��״̬������ƽ���ǻ�ѧƽ���һ�֣�ͬ�����л�ѧƽ��������������ı�ʱƽ���ƶ��Ĺ��ɷ�����ɳ����ԭ��������ȷ�����⣮

 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д�