题目内容
(共9分,每小题3分)常温下,在27.5g水中溶解12.5g CuSO4·5H2O,恰好达到饱和,该溶液密度为1.21g /cm3,求:
①该溶液中阴阳离子的总物质的量 ②该溶液中CuSO4的物质的量浓度
③取出20.0 ml该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?(计算过程规范)
①该溶液中阴阳离子的总物质的量 ②该溶液中CuSO4的物质的量浓度
③取出20.0 ml该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?(计算过程规范)
① 0.100 mol(3分) ② 1.51 mol /·L(3分) ③ 30.2 ml(3分)
考查物质的量的有关计算。
①胆矾的摩尔质量是250g/mol
所以根据n=m/M可知,12.5g胆矾的质量是12.5g÷125g/mol=0.05mol
根据胆矾的化学式可知,溶液中铜离子和SO42-的物质的量都是0.05mol/L
所以溶液中阴阳离子总的物质的量是0.05mol×2=0.100mol
②溶液的质量是27.5g+12.5g=40g
溶液的密度是1.21g/ml
所以溶液的体积是40g÷1.21g/ml=33.06ml
因此根据c=n/V可知,溶液的浓度是0.05mol÷0.03306L=1.51mol/L
③由于在稀释过程中溶质是不变的,所以稀释后溶液的体积是
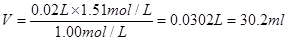
①胆矾的摩尔质量是250g/mol
所以根据n=m/M可知,12.5g胆矾的质量是12.5g÷125g/mol=0.05mol
根据胆矾的化学式可知,溶液中铜离子和SO42-的物质的量都是0.05mol/L
所以溶液中阴阳离子总的物质的量是0.05mol×2=0.100mol
②溶液的质量是27.5g+12.5g=40g
溶液的密度是1.21g/ml
所以溶液的体积是40g÷1.21g/ml=33.06ml
因此根据c=n/V可知,溶液的浓度是0.05mol÷0.03306L=1.51mol/L
③由于在稀释过程中溶质是不变的,所以稀释后溶液的体积是
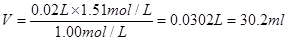

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目