题目内容
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
|
|
|
|
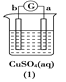
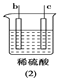
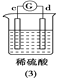
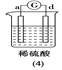
a极质量减小,b极质量增加 | b极有气体产生,c极无变化 | d极溶解,c极有气体产生 | 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是
A. d>a>b>cB. b>c>d>aC. a>b>c>dD. a>b>d>c
【答案】A
【解析】
第一个装置中a极质量减小,b极质量增加,说明金属活动性a>b;
第二个装置没有形成原电池,由于b极有气体产生,c极无变化,说明b可以置换酸中的H,c不能置换酸中的H,所以金属活动性b>c;
根据第三个装置中,构成了原电池,其中d极溶解,c极有气体产生,说明金属活动性d>c;第四个装置中,由于规定正电荷移动方向为电流方向,电流从a极流向d极,则金属活动性d>a,综上所述,可知金属活动性有强到弱的顺序是d>a>b>c。
故合理选项是A。

练习册系列答案
相关题目