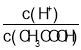题目内容
【题目】某化学研究小组探究外界条件对化学反应速率和化学平衡、溶液pH影响的图像,其中图像和实验结论表达均正确的是

A.①是其他条件一定时,反应速率随温度变化的图像,正反应△H<0
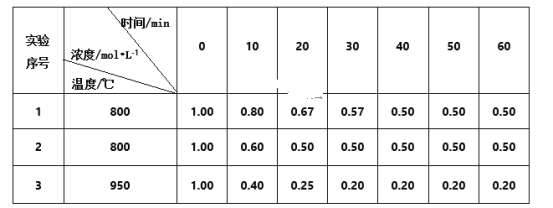
B.②是在平衡体系的溶液中加入少量KCl晶体后化学反应速率随时间变化的图像
C.③是在有无催化剂存在下建立的平衡过程图像,a是使用催化剂时的曲线
D.④是表示Cl2通入H2S溶液中pH变化
【答案】C
【解析】
A.由图知,在v正等于v逆之后,v正大于v逆,则随着温度升高,反应平衡向正方向移动,可得△H>0,A项错误;
B.该反应实质为Fe3+ + 3SCN- Fe(SCN)3,在平衡体系的溶液中加入少量KCl晶体,对该反应无任何影响,B项错误;
C. 由图知,a、b曲线中A的体积分数不变,说明改变条件不发生平衡移动,且a情况下,化学反应速率更快,则a是使用催化剂时的曲线,C项正确;
D. 由Cl2 + H2S = 2HCl +S↓知:溶液由弱酸H2S逐渐变为强酸HCl,溶液pH值从开始反应起会越来越小,D项错误;
故选C。

练习册系列答案
相关题目