题目内容
【题目】某实验小组设计实验制备NaHSO2·HCHO·2H2O[次硫酸氢钠甲醛(雕白块)]。回答下列问题:
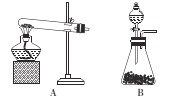
⑴甲同学用下列装置制备实验原料Na2S2O5(焦亚硫酸钠),装置如图:
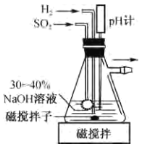
已知pH=4.1的过饱和NaHSO3溶液能自动脱水生成Na2S2O5。
①通入H2的目的是___。
②通入SO2发生反应的化学方程式依次为___、___和2NaHSO3=Na2S2O5↓十H2O。
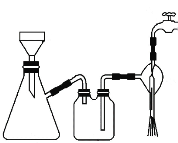
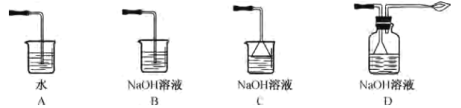
③从环境保护和安全考虑,尾气处理方法正确的是___ (填字母)。
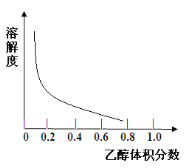
④实验若用稀NaOH溶液,则不能制得Na2S2O5,其原因是___。
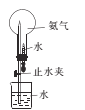
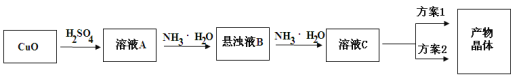
⑵乙同学用甲同学制得的Na2S2O5通过下列装置(夹持装置已略)合成雕白块。
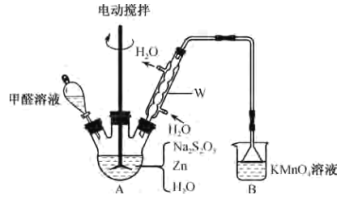
①仪器W的名称是___。
②合成反应温度需保持在75℃,采用的合适加热方式是___,已知反应中Zn转化为ZnO和Zn(OH)2,三口烧瓶中发生反应的化学方程式为___。
③三口烧瓶中的反应液需经过过滤、___、过滤、洗涤及干燥,得雕白块。
【答案】排除系统内空气 2NaOH+SO2=Na2SO3+H2O SO2+Na2SO3+H2O=2NaHSO3 D 不能得到NaHSO3过饱和溶液 (球形)冷凝管 热水浴 Na2S2O3+2Zn+2HCHO+6H2O![]() 2[NaHSO2HCHO2H2O]+ZnO+Zn(OH)2 蒸发浓缩、冷却结晶
2[NaHSO2HCHO2H2O]+ZnO+Zn(OH)2 蒸发浓缩、冷却结晶
【解析】
Na2S2O5(焦亚硫酸钠)易被氧化,先将装置内空气排出,再通入二氧化硫与氢氧化钠溶液反应生成亚硫酸钠,继续通入生成亚硫酸氢钠,得到饱和亚硫酸氢钠,自然脱水得到Na2S2O5(焦亚硫酸钠),再将Na2S2O5(焦亚硫酸钠)与Zn、HCHO溶液在水浴中加热反应生成ZnO、Zn(OH)2、NaHSO2HCHO2H2O,经过过滤,再将滤液蒸发浓缩、冷却结晶、过滤得产品。
⑴①Na2S2O5(焦亚硫酸钠)容易被氧化,因此通入H2的目的是排除系统内空气;故答案为:排除系统内空气。
②通入SO2,二氧化硫和氢氧化钠反应生成亚硫酸钠和水,亚硫酸钠和二氧化硫反应生成亚硫酸氢钠,反应依次为2NaOH+SO2=Na2SO3+H2O、2NaOH+SO2 =Na2SO3+H2O和2NaHSO3=Na2S2O5↓十H2O;故答案为:2NaOH+SO2 = Na2SO3+H2O;2NaOH+SO2=Na2SO3+H2O。
③从环境保护和安全考虑,二氧化硫会污染环境,用氢氧化钠溶液处理,要注意防倒吸,氢气用点燃方法进行处理,因此尾气处理方法正确的是D;故答案为:D。
④根据题中信息pH=4.1的过饱和NaHSO3溶液能自动脱水生成Na2S2O5,因此用稀NaOH溶液不能得到NaHSO3过饱和溶液;故答案为:不能得到NaHSO3过饱和溶液。
⑵①根据图中信息得到仪器W的名称是(球形)冷凝管;故答案为:(球形)冷凝管。
②合成反应温度需保持在75℃,温度低于100℃,且控制温度,因此采用的合适加热方式是热水浴,已知反应中Zn转化为ZnO和Zn(OH)2,三口烧瓶中发生反应的化学方程式为Na2S2O3+2Zn+2HCHO+6H2O![]() 2[NaHSO2HCHO2H2O]+ZnO+Zn(OH)2;故答案为:热水浴;Na2S2O3+2Zn+2HCHO+6H2O
2[NaHSO2HCHO2H2O]+ZnO+Zn(OH)2;故答案为:热水浴;Na2S2O3+2Zn+2HCHO+6H2O![]() 2[NaHSO2HCHO2H2O]+ZnO+Zn(OH)2。
2[NaHSO2HCHO2H2O]+ZnO+Zn(OH)2。
③三口烧瓶中的反应液需经过过滤,滤液为雕白块溶液,将溶液蒸发浓缩、冷却结晶、过滤、洗涤及干燥,得雕白块;故答案为:蒸发浓缩、冷却结晶。

 阅读快车系列答案
阅读快车系列答案【题目】氯气是一种重要的工业原料,液氯储存区贴有的说明卡如下:
包装 | 钢瓶 |
储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
泄漏处理 | NaOH、NaHSO3溶液吸收 |
下列解释事实的方程式不正确的是
A. 氯气用于自来水消毒:Cl2 + H2O![]() 2H+ + Cl-+ ClO-
2H+ + Cl-+ ClO-
B. 电解饱和食盐水制取Cl2:2Cl- +2H2O![]() 2OH-+ H2↑+Cl2↑
2OH-+ H2↑+Cl2↑
C. 浓氨水检验泄露的氯气,产生白烟:8NH3 + 3Cl2 === 6 NH4Cl + N2
D. 氯气“泄漏处理”中NaHSO3溶液的作用:HSO3-+ Cl2 + H2O === SO42-+ 3H+ + 2Cl-
【题目】目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行了探究。己知在不同温度下的化学平衡常数(K1、K2、K3)如表所示。
化学反应 | 焓变 | 平衡常数 | 温度/℃ | ||
500 | 700 | 800 | |||
①2H2(g)+CO(g) | △H1 | K1 | 2.5 | 0.34 | 0.15 |
②CO2(g)+H2(g)CO(g)+H2O(g) | △H2 | K2 | 1.0 | 1.70 | 2.52 |
③CO2(g)+3H2(g)CH3OH(g)+H2O(g) | △H3 | K3 | |||
请回答下列问题:
(1)反应②是_______(填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=_______(用K1、K2表示);根据反应③判断△S_______(填“>”“=”或“<”)0,在_______(填“较高”或“较低”)温度下有利于该反应自发进行。
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有______(填字母,后同)。
A.缩小反应容器的容积 B.增大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.从平衡体系中及时分离出CH3OH
(4)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g的浓度分别为 0.1mol/L、0.8 mol/L、0.3 mol/L、0.15 mol/L,则此时v(正)_______v(逆) (填“>”“=”或“<”)。
(5)某兴趣小组研究反应②的逆反应速率在下列不同条件下随时间的变化曲线,开始时升高温度,t1时平衡,t2时减小压强,t3时增大CO的浓度,t4时又达到平衡。在下图中画出t2至t4的曲线。_____