题目内容
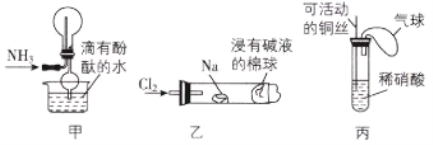
【题目】二氧化硫通入氯化钡溶液中理论上不产生沉淀,而实际受到空气和溶液中氧气的影响很快便能观察到沉淀现象。为了避免产生沉淀,某化学小组设计了如下实验装置,实验操作步骤如下:

①气密性检査完好后,在装置A中的多孔隔板上放上锌粒,通过_______注入稀硫酸、打开活塞,将产生的氢气导入到后续装置。
②________后,关闭活塞,将装置D的导管插入烧杯中。
③通过装置B的________滴加浓硫酸,产生的气体进入到BaCl2溶液中,溶液保持澄清。
④打开活塞,将产生的氢气导入后续装置一段时间。
⑤将盛有BaCl2溶液的试管从装置中取出,拔去橡皮塞用胶头滴管伸入到苯层下方滴加双氧水,随即出现白色浑浊,滴加稀盐酸并振荡,白色浑浊不消失。
⑥拆卸装置,清洗仪器,处理剩余药品。
请回答下列问题:
(1)实验步骤①和③的空白处使用的仪器分别为__________、__________
(2)装置C中苯的作用是__________。
(3)实验步骤②的操作为__________。
(4)实验步骤④的目的是__________。
(5)写出实验步骤⑤试管中发生反应的化学方程式:__________、____________。
(6)为了避免产生沉淀,你认为还应采取哪些措施?请举一例:__________。
【答案】长颈漏斗 分液漏斗 将BaCl2溶液与空气隔离 将装置D的导管口向上,用试管收集满氢气并验纯, 待氢气纯净 将装置内残留的二氧化硫全部转移到氢氧化钠溶液中吸收,以防止污染 SO2+H2O2=H2SO4 H2SO4+BaCl2=BaSO4 ↓ +2HCl 将BaCl2溶液煮沸
【解析】
(1)长颈漏斗无盖子和旋塞,可以作为加入液体反应物的仪器;分液漏斗的结构和长颈漏斗有很大从差异,有盖有旋塞,注意结合物质的性质采用不同的加入液体的仪器;
(2)苯密度比水小,在氯化钡溶液的上层,可以起到隔离空气的作用;
(3)装置获取氢气的作用是将装置中的气体赶尽,防止二氧化硫通入氯化钡溶液后的现象受到空气和溶液中氧气的影响,待氢气纯净后方可将二氧化硫通入氯化钡溶液;
(4)二氧化硫有毒能造成大气污染;
(5)双氧水具有氧化性,可以将二氧化硫氧化为硫酸,硫酸与氯化钡反应产生硫酸钡沉淀;
(6)实验要进行顺利必须要隔绝氧气的干扰。
(1)可以通过长颈漏斗实现锌粒和酸的接触,装置B为分液漏斗;
(2)装置C中在溶液液面上覆盖一层苯,由于苯密度比水小,在氯化钡溶液的上层,可以起到隔离空气的作用;
(3)A装置获取氢气的作用是将装置中的气体赶尽,待氢气纯净后再将二氧化硫通入氯化钡溶液中;
(4)二氧化硫有毒,为了防止造成污染,在实验结束时要再次打开活塞,将产生的氢气导入后续装置一段时间,让SO2全部被氢氧化钠吸收,以防止污染;
(5)双氧水具有强的氧化性,可以将二氧化硫氧化为硫酸,硫酸和氯化钡反应生成沉淀,由于硫酸钡既不溶于水,也不溶于酸,因此产生白色沉淀后,再滴加稀盐酸并振荡,白色浑浊不消失。有关反应方程式为:SO2+H2O2=H2SO4,H2SO4+BaCl2=BaSO4↓ +2HCl;
(6)实验要隔绝空气中的氧气,除去氧气的方法很多,如将BaCl2溶液煮沸以驱赶其中的氧气;或者加入植物油等不溶于水且密度小于水的有机物。

【题目】(1)0.3 mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5 kJ热量,其热化学方程式为____。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式为2NO+2CO![]() 2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/s | 0 | 1 | 2 |
c(NO)/ mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 |
c(CO)/mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 |
时间/s | 3 | 4 | 5 |
c(NO)/ mol·L-1 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO)/ mol·L-1 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答下列问题:
①前2s内的平均反应速率υ(N2)=____;
②上述条件下,该反应的平衡常数为____;
③上述条件下,测得某时刻反应体系中各物质的物质的量浓度均为0.01 mol/L,则此时反应处于____状态。(填“平衡”或“向右进行”或“向左进行”)
(3)实验室常用0.10 mol/L KMnO4标准酸性溶液来测定H2C2O4样品的纯度(标准液滴待测液),其反应原理为:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O。
①KMnO4标准液应装在____(填“酸式”或“碱式”)滴定管;
② 清水洗净滴定管后直接装入标准液,则测定结果会____;(填“偏大”或“偏小”或“不变”)
③ 滴定过程中发现一段时间后反应速率明显加快,除去温度的影响,你认为最有可能的原因是____。