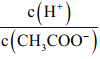题目内容
【题目】下表列出了A~R 9种元素在周期表中的位置:(用元素符号回答)
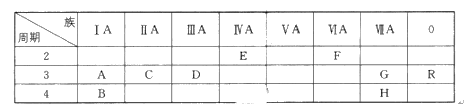
(1)这9种元素其中化学性质最不活泼的是________;
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是_______________;
(3)A、B、C三种元素按原子半径由大到小的顺序排列为________;
(4)F元素氢化物的化学式是________,
【答案】ArAl(OH)3+OH-=AlO2-+2H2OK>Na>MgH2O和H2O2
【解析】
由元素在周期表中的位置可知,A为Na元素,B为K元素,C为Mg元素,D为Al元素,E为C元素,F为O元素,G为Cl元素,H为Br元素,R为Ar元素。
(1)元素周期表中稀有气体元素化学性质最不活泼。
(2)Al(OH)3是一种难溶于水的碱,具有两性,与氢氧化钠溶液反应,生成偏铝酸钠和水。
(3)一般电子层越多,半径越大;电子层相同,原子序数越大半径越小。
(4)氧元素的氢化物有水和过氧化氢两种。
(1)以上几种元素中,稀有气体元素Ar原子最外层为稳定结构,化学性质最不活泼。
(2)D为Al元素,其最高价氧化物对应的水化物为Al(OH)3,与氢氧化钠溶液反应,生成偏铝酸钠和水,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O。
(3)A为Na元素,B为K元素,C为Mg元素,因为同主族元素原子,电子层越多,半径越大,同周期元素原子序数大的半径小,所以原子半径由大到小的顺序排列为K>Na>Mg。
(4)F为O元素,其氢化物为水和过氧化氢,化学式是H2O和H2O2。

【题目】可逆反应aA(g)+bB(s)cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是 ( )
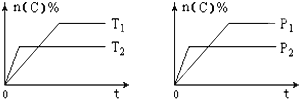
A. P1 > P2
B. 该反应的ΔH < 0
C. 化学方程式系数a>c+d
D. 使用催化剂,C的物质的量分数增加
【答案】B
【解析】A.先拐先平数值大,由右图可知,P2>P1,故A错误;B. 先拐先平数值大,由左图可知,T2>T1,升高温度C的物质的量分数减小,说明升高温度平衡逆向移动,则该反应为放热反应,ΔH < 0,故B正确;C. 由右图可知,P2>P1,增大压强C的物质的量分数减小,说明增大压强平衡逆向移动,则逆反应方向为气体体积减小的方向,所以化学方程式系数a<c+d,故C错误;D. 使用催化剂不能使化学平衡发生移动,则C的物质的量分数不变,故D错误;答案选B。
【题型】单选题
【结束】
22
【题目】25℃时,0.1 molL-1溶液的pH如下表,下列有关说法正确的是 ( )
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
pH | 7.0 | 7.0 | 8.1 | 8.4 |
A. 酸性强弱:HF<H2CO3
B. ①和②中溶质均未水解
C. 由水电离产生的c(H+):①>②
D. ④溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)= c(Na+)